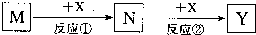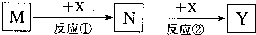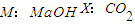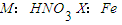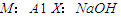解:D是石油化工的重要基础原料,也是一种植物生长调节剂,所以D是乙烯;D、L是相对分子质量相等的两种气体,且含有同一种元素,则L是CO或氮气;在加热、浓硫酸作催化剂条件下,乙醇发生消去反应生成乙烯和水,所以A是乙醇,E是水;B是无色气体单质,乙醇燃烧生成二氧化碳和水,所以F是二氧化碳;
H与J反应生成的溶液遇苯酚显紫色,则H和J反应的生成物是铁盐,②、③、④都是工业生产中的重要反应,B是氧气,则C中含有铁元素,G和氧气能反应,I和水能反应,铁的化合物和水不反应,则I的非金属氧化物,为酸性氧化物,H和L反应,反应条件是同温,氮气和氢气的反应条件是高温、高压、催化剂,所以是H和一氧化碳发生氧化还原反应,则H是铁的氧化物,高温条件下和铁的化合物反应生成氧化铁及酸性氧化物的物质是FeS
2,所以C是FeS
2,G是二氧化硫,I是三氧化硫,J是硫酸,H是氧化铁,氧化铁和一氧化碳反应生成铁和二氧化碳,所以L是CO,K和M一种是铁一种是二氧化碳.
(1)通过以上分析知,C是FeS
2,D是乙烯,电子式为
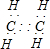
,故答案为:FeS
2;
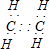
;
(2)乙烯中含有碳碳双键,能和溴发生加成反应,二氧化硫有还原性,能和溴发生氧化还原反应,所以乙烯和二氧化硫都能使溴水褪色,
故答案为:C
2H
4、SO
2;
(3)170℃,浓硫酸作催化剂的条件下,乙醇发生消去反应生成乙烯和水,反应方程式为C
2H
5OH
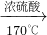
C
2H
4↑+H
2O,
故答案为:C
2H
5OH
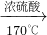
C
2H
4↑+H
2O;
(4)氧化铁和稀硫酸反应生成氯化铁和水,离子反应方程式为Fe
2O
3+6H
+=2F
3++3H
2O,故答案为:Fe
2O
3+6H
+=2F
3++3H
2O;
(5)生成1mol三氧化硫放出98.3lkJ的热量,则生成2mol三氧化硫放出196.6kJ热量,所以该反应的热化学反应方程式为
2SO
2(g)+O
2(g)
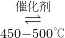
2SO
3(g)△H=-196.6kJ/mol,该反应在接触室中进行,该反应是气体体积减小的、放热反应,增大压强、降低温度有利于平衡向正反应方向移动,但常压下该反应已经达到90%的转化率,且高压对设备要求更高,提高的转化率不大,温度较低时反应速率较小不利于工业生产,为提高反应速率用五氧化二钒作催化剂,
故答案为:2SO
2(g)+O
2(g)
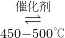
2SO
3(g)△H=-196.6kJ/mol;接触室;常压、450-500℃、五氧化二钒作催化剂.
分析:D是石油化工的重要基础原料,也是一种植物生长调节剂,所以D是乙烯;D、L是相对分子质量相等的两种气体,且含有同一种元素,则L是CO或氮气;在加热、浓硫酸作催化剂条件下,乙醇发生消去反应生成乙烯和水,所以A是乙醇,E是水;B是无色气体单质,乙醇燃烧生成二氧化碳和水,所以F是二氧化碳;
H与J反应生成的溶液遇苯酚显紫色,则H和J反应的生成物是铁盐,②、③、④都是工业生产中的重要反应,B是氧气,则C中含有铁元素,G和氧气能反应,I和水能反应,铁的化合物和水不反应,则I的非金属氧化物,为酸性氧化物,H和L反应,反应条件是同温,氮气和氢气的反应条件是高温、高压、催化剂,所以是H和一氧化碳发生氧化还原反应,则H是铁的氧化物,高温条件下和铁的化合物反应生成氧化铁及酸性氧化物的物质是FeS
2,所以C是FeS
2,G是二氧化硫,I是三氧化硫,J是硫酸,H是氧化铁,氧化铁和一氧化碳反应生成铁和二氧化碳,所以L是CO,K和M一种是铁一种是二氧化碳.
点评:本题以化合物的推断为载体考查了元素化合物的性质,正确推断元素化合物是解本题的关键,注意用乙醇制取乙烯的反应中温度控制在170℃,如果在140℃,则生成乙醚.

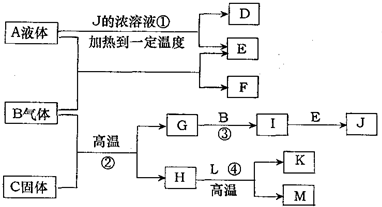 A-M有如图转化关系.已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色.(有些反应条件已省略)
A-M有如图转化关系.已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色.(有些反应条件已省略)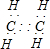 ,故答案为:FeS2;
,故答案为:FeS2;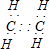 ;
;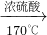 C2H4↑+H2O,
C2H4↑+H2O,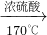 C2H4↑+H2O;
C2H4↑+H2O;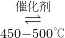 2SO3(g)△H=-196.6kJ/mol,该反应在接触室中进行,该反应是气体体积减小的、放热反应,增大压强、降低温度有利于平衡向正反应方向移动,但常压下该反应已经达到90%的转化率,且高压对设备要求更高,提高的转化率不大,温度较低时反应速率较小不利于工业生产,为提高反应速率用五氧化二钒作催化剂,
2SO3(g)△H=-196.6kJ/mol,该反应在接触室中进行,该反应是气体体积减小的、放热反应,增大压强、降低温度有利于平衡向正反应方向移动,但常压下该反应已经达到90%的转化率,且高压对设备要求更高,提高的转化率不大,温度较低时反应速率较小不利于工业生产,为提高反应速率用五氧化二钒作催化剂,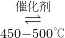 2SO3(g)△H=-196.6kJ/mol;接触室;常压、450-500℃、五氧化二钒作催化剂.
2SO3(g)△H=-196.6kJ/mol;接触室;常压、450-500℃、五氧化二钒作催化剂.

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案