
| A. | C+O2═CO2 | B. | NH3+HCl═NH4Cl | ||
| C. | 2Fe(OH)3═Fe2O3+3H2O | D. | NaOH+HNO3═NaNO3+H2O |
分析 判断物质发生反应时,所含元素的化合价是否发生变化,如化合价发生变化,则发生氧化还原反应,不变化,则不涉及氧化还原反应.
解答 解:A.C+O2═CO2,存在化合价的变化,为氧化还原反应,故A选;
B.NH3+HCl═NH4Cl,没有化合价的变化,不是氧化还原反应,故B不选;
C.2Fe(OH)3═Fe2O3+3H2O,没有化合价的变化,不是氧化还原反应,故C不选;
D.NaOH+HNO3═NaNO3+H2O,没有化合价的变化,不是氧化还原反应,故D不选.
故选A.
点评 本题考查氧化还原反应,题目难度不大,本题注意根据元素的化合价变化分析判断,注重基础知识的积累,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 绿色食品就是不含任何化学物质的食品 | |
| B. | 燃煤时添加生石灰以减少SO2的排放 | |
| C. | PM2.5是指环境空气中直径小于或等于2.5微米的颗粒物 | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
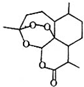 屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | B. | 青蒿素是芳香族化合物 | ||
| C. | 青蒿素可以发生水解反应 | D. | 青蒿素不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )具有高度的对称性,Eaton教授在此基础上经七步反应合成了二羧基立方烷,二羧基立方烷的同分异构体数目为( )
)具有高度的对称性,Eaton教授在此基础上经七步反应合成了二羧基立方烷,二羧基立方烷的同分异构体数目为( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
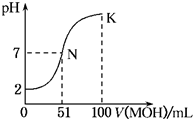 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 脱氧过程是吸热反映,可降低温度,延长糕点保质期 | |
| B. | 脱氧过程中铁作原电池负极,电极反应为:Fe-3e-→Fe3+ | |
| C. | 脱氧过程中热能转化为生成物的内部能量 | |
| D. | 标准状况能吸收氧气336mL,理论上最少要含有1.12g铁粉的脱氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫是黄色能溶于水的晶体 | |
| B. | 臭氧空洞的形成主要与SO2有关 | |
| C. | 硫在自然界仅以化合态存在 | |
| D. | 硫既能与某些金属反应又能与某些非金属反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com