
下列物质分类的正确组合是
混合物 | 化合物 | 单质 | 盐 | |
A | 盐酸溶液 | NaOH溶液 | 石墨 | 食盐 |
B | 水玻璃 | KNO3晶体 | O3 | 纯碱 |
C | 氢氧化铁胶体 | 澄清石灰水 | 铁 | 石灰石 |
D | CuSO4·5H2O | CaCl2 | 水银 | CaO |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:2014-2015学年山东省高三元月模拟测试化学试卷(解析版) 题型:选择题
下列与氯有关的说法中,正确的是
A.通过化学变化可以实现35Cl与37Cl间的相互转化
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移1mol电子
查看答案和解析>>
科目:高中化学 来源:2014--2015吉林省高一上学期期末化学试卷(解析版) 题型:选择题
相同质量的下列气体,在同温同压下占有的体积最大的是
A.H2 B.O2 C.Cl2 D.SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一1月月考化学试卷(解析版) 题型:选择题
以下物质间的每步转化通过一步反应就能实现的是
A.Al- Al2O3- Al(OH)3- NaAlO2 B.Mg- MgCl2- Mg(OH)2- MgO
C.S- SO3- H2SO4- MgSO4 D.Si- SiO2- H2SiO3 - Na2 SiO3
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一1月月考化学试卷(解析版) 题型:选择题
归纳与推理是化学学习常用的方法。下列推理正确的是
A.因为稀硫酸能与铁反应放出H2,所以浓硫酸与铁反应也一定能放出H2
B.因为Na可以与水反应放出H2,所以K也可以与水反应放出H2
C.因为CO2的水溶液可以导电,所以CO2是电解质
D.因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二1月月考化学试卷(解析版) 题型:选择题
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.1 mol·L-1 CuSO4·(NH4)2SO4·6H2O的溶液中:c(SO42—)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-)
C.0.1 mol·L-1 NaHSO3溶液中:c(H+)+c(H2SO3)=c(SO32—)+c(OH-)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二1月月考化学试卷(解析版) 题型:选择题
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g) + I2(?) 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
A.①中的I2为固态,②中的I2为气态
B.②的反应物总能量比①的反应物总能量低
C.①的产物比②的产物热稳定性更好
D.1 mol固态碘升华时将吸热17 kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
关于氯化铁水解的错误说法是
A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动
B.浓度为5mol/L和0.5mol/L的两种FeCl3溶液,其它条件相同时,Fe3+的水解程度前者比后者低
C.有50℃和20℃的相同浓度氯化铁溶液,其他条件相同时,Fe3+的水解程度前者比后者小
D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:填空题
(10分)I、常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

回答下列问题:
(1)在同一溶液中,H2CO3、HCO3-、CO32-(填:“能”或“不能”) 大量共存。
(2)已知在25℃时,CO32-水解反应的平衡常数(即水解常数用Kh表示)
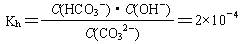
当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
(3)当混合液的pH=________时,开始放出CO2气体。
II、(1)常温下向25mL含HCl 0.01mol的溶液中滴加氨水至过量,该过程中水的电离平衡____________________(填写电离平衡移动情况)。当滴加氨水到25mL时,测得溶液中水的电离度最大,则氨水的浓度为______________。
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________7(填“>”、“<”或“=”)。
(3)25 ℃时,将a mol NH4NO3溶于水,向所得溶液中滴加b L氨水后溶液呈中性,则所滴加氨水的浓度是________mol·L-1。(用含a 、b 的式子表示)(NH3·H2O的电离平衡常数取Kb=2×10-5 mol·L-1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com