
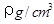 ,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为
,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的摩尔质量可以表示为 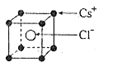
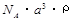 g/mol B.
g/mol B.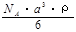 g/mol
g/mol 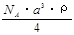 g/mol D.
g/mol D.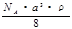 g/mol
g/mol| 元素编号 | 元素性质或原子结构 |
| A | 原子的电子排布图为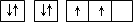 |
| B | 常温下单质为双原子分子,原子间形成三对共用电子对 |
| C | 原子的s轨道电子数等于p轨道电子数,元素的最低负价为-2价 |
| D | 二价阳离子与C的阴离子具有相同的电子层结构 |
| E | 原子序数是D两倍, |
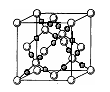
 ,所以选项A正确。
,所以选项A正确。

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铍(Be)是一种金属,它的最高价氧化物的水化物可能具有两性 |
| B.砹是一种有色固体,HAt不稳定,AgAt是有色难溶于水的固体 |
| C.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X是第ⅠA元素,Z是第ⅦA元素 |
| B.X、Y、Z三种元素的最高化合价依次升高 |
| C.Z的最高价氧化物对应的水化物是强酸 |
| D.如果Y的最高价氧化物的水化物难溶于水,则Y一定是Al |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
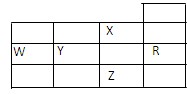
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.最高价含氧酸的酸性,Y对应的酸性强于W |
| D.P能级未成对电子最多的是Z元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.x的原子半径大于y的原子半径 |
| B.x的第一电离能小于y 的第一电离能 |
| C.x的金属性大于y的金属性 |
| D.x的电负性大于y的电负性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| a | | | |||||
| | | | b | c | d | | |
| e | | f | | | g | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com