
【题目】下图是某研究性学习小组设计的对一种废旧合金各成分(含有Cu、Fe、Si 三种成分)进行分离、回收再利用的工业流程,通过该流程能得到常用的单质、聚铁(碱式硫酸铁的聚合物)、铁红(Fe2O3)和绿矾(FeSO4·7H2O)。
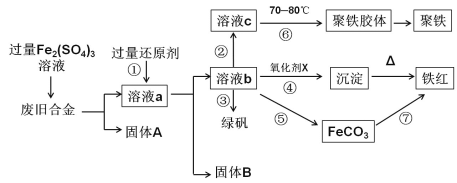
(1)加入过量Fe2(SO4)3溶液过程中与较活泼的金属反应的离子方程式: 。
(2)①中过量的还原剂应是 ,固体B是 。
(3)向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为
(4)②中加入H2O2,并调节pH值得到溶液c,在⑥中,将溶液c控制到70~80 ℃的目的是 。
(5)在③中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有 。
(6)在④中的氧化剂X是 。
(7)在⑤中,向溶液b加入了NH4HCO3溶液,得到FeCO3沉淀,写出其离子反应方程式: 。
(8)在⑦中,写出FeCO3煅烧的化学反应方程式: 。
【答案】(1)2Fe3++Fe=3Fe2+
(2)铁粉(Fe)(1分)。铁粉、铜粉(Fe、Cu)。
(3)MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(4)升高温度促进Fe3+的水解,过高温度不利于聚铁的形成(或者完全水解了)
(5)蒸发皿、玻璃棒
(6)Na2O2或NaClO(或其它合理答案)
(7)Fe2++2HCO3-=FeCO3↓+CO2↑+H2O
(8)FeCO3+O2![]() 2Fe2O3+4CO2↑
2Fe2O3+4CO2↑
【解析】
试题分析:(1)加入过量Fe2(SO4)3溶液能与Fe和Cu反应,铁较活泼,反应的离子方程式2Fe3+ + Fe = 3Fe2+;(2)根据流程,a含有Fe2+、Fe3+、Cu2+,加入还原剂后,a溶液中只含有Fe2+,所以①中过量的还原剂应是铁,固体B是铜;(3) 向溶液b中含有Fe2+,加入酸性KMnO4溶液发生反应的离子方程式为MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O;(4)向溶液b中含有Fe2+,中加入H2O2,把Fe2+氧化为Fe3+,Fe3+易水解在⑥中,将溶液c控制到70~80 ℃的目的是升高温度促进Fe3+的水解 ,过高温度不利于聚铁的形成;(5)蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有蒸发皿 、玻璃棒;(6)根据流程图,在④中的氧化剂X是Na2O2;(7)向溶液硫酸亚铁溶液中加入了NH4HCO3溶液,得到FeCO3沉淀,其离子反应方程式Fe2+ + 2HCO3- = FeCO3↓ + CO2↑+ H2O;(8)FeCO3煅烧生成氧化铁,化学反应方程式FeCO3+O2![]() 2Fe2O3+4CO2↑。
2Fe2O3+4CO2↑。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三支试管,分别加入下列物质后,观察三支试管的颜色,其中颜色最浅的是
甲:10mL0.01mol·L-1的FeCl3溶液和10mL0.01mol·L-1的KSCN溶液
乙:5mL水、10mL0.01mol·L-1的FeCl3溶液5mL0.01mol·L-1的KSCN溶液
丙:10mL0.1mol·L-1的FeCl3,溶液和10mL0.1mol·L-1的KSCN溶液
A. 甲试管 B. 乙试管 C. 丙试管 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由锌片、铜片和200 mL稀H2SO4组成的原电池如图所示。
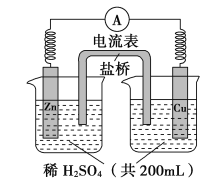
(1)原电池的负极反应是______________________,
正极反应是__________________________。
(2)电流的方向是_____________。
(3)一段时间后,当在铜片上放出1.68 L(标准状况下)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗________g锌,有____________个电子通过了导线,原硫酸的物质的量浓度是_____________(设溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁。这现象说明了( )
A.该反应是吸热反应 B.铁粉和硫粉在常温下可以发生反应
C.该反应是放热反应 D.硫化亚铁的总能量高于铁粉和硫粉的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.10g镁铝合金加入120mL4.0mol·L-1的盐酸中,待合金完全溶解后,得到溶液X。下列说法一定正确的是
A. 合金完全溶解后产生的H2的物质的量为0.24mol
B. 合金中的镁与铝的物质的量之比小于1
C. 若向溶液X中加入270mL2.0mol·L-1NaOH溶液,充分反应,所得沉淀为Mg(OH)2
D. 若向溶液X中加入足量的氨水,充分反应,所得沉淀经过过滤、洗涤后充分灼烧,则残留固体质量大于8.50g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是 ( )
A. 在催化剂存在条件下苯与液溴反应制溴苯
B. 苯与浓硝酸、浓硫酸混合共热制取硝基苯
C. 苯与浓硫酸共热制取苯磺酸
D. 在一定条件下苯与氢气反应制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把100 mL含有CaCl2和KCl的混合溶液分成2等份,取一份加入含amol碳酸钠的溶液,恰好使钙离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A. 20(b-2a) mol/L B. 10(2a-b) mol/L
C. 20(b-a) mol/L D. 0.1(b-2a) mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com