
 CH3OH(g) △H= -90.8kJ/mol
CH3OH(g) △H= -90.8kJ/mol CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol CO2(g)+H2(g) △H=-41.3kJ/mol
CO2(g)+H2(g) △H=-41.3kJ/mol CH3OCH3(g)+CO2(g) 的△H= ;
CH3OCH3(g)+CO2(g) 的△H= ; CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
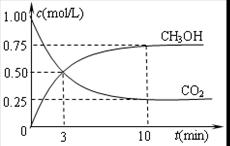
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度(mol·L-1) | 0.40 | 0.6 | 0.6 |
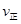 _________
_________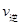 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。 CH3OCH3(g)+CO2(g) △H=2×(-90.8kJ/mol)+(-23.5kJ/mol)+(-41.3kJ/mol)=-246.4 kJ/mol。(2)若a压缩体积,体系的压强增大,化学平衡向正反应方向移动,反应物的转化率提高;b加入催化剂能同等倍数改变正、逆反应的化学反应速率,缩短达到平衡所需时间,平衡不移动;c减少CO2的浓度,平衡向正反应方向移动,反应物的转化率提高;d.增加CO的浓度,平衡向正反应方向移动,但增加量远远大于平衡移动消耗量,所以CO的转化率反而降低。e.分离出二甲醚(CH3OCH3)即减小生成物的浓度,化学平衡向正反应方向移动,反应物的转化率提高。故在该总反应中,要提高CO的转化率的途径是ace.(2)①比较常数各生成物浓度幂指数乘积与反应物浓度幂指数乘积的比与K 大小。如果比K大,平衡向逆反应方向移动,V逆>V正;如果比K小,平衡向正反应方向移动, V正>V逆;如果等于K,平衡不会发生移动, V正=V逆;由于(0.6×0.6)/(0.4)2==9/4<400,所以平衡向正反应方向移动,V正>V逆。②化学平衡常数是可能反应达到化学平衡时隔生成物浓度幂指数的乘积与各反应物浓度幂指数的乘积的比即K={C(CH3OCH3)×C(H2O)} /C2(CH3OH).该反应的正反应是放热反应,升高温度,根据勒夏特列原理,化学平衡向逆反应方向移动,生成物的浓度减小,反应物的浓度增大,对化学平衡常数来说,分子减小,分母扩大,所以K减小。
CH3OCH3(g)+CO2(g) △H=2×(-90.8kJ/mol)+(-23.5kJ/mol)+(-41.3kJ/mol)=-246.4 kJ/mol。(2)若a压缩体积,体系的压强增大,化学平衡向正反应方向移动,反应物的转化率提高;b加入催化剂能同等倍数改变正、逆反应的化学反应速率,缩短达到平衡所需时间,平衡不移动;c减少CO2的浓度,平衡向正反应方向移动,反应物的转化率提高;d.增加CO的浓度,平衡向正反应方向移动,但增加量远远大于平衡移动消耗量,所以CO的转化率反而降低。e.分离出二甲醚(CH3OCH3)即减小生成物的浓度,化学平衡向正反应方向移动,反应物的转化率提高。故在该总反应中,要提高CO的转化率的途径是ace.(2)①比较常数各生成物浓度幂指数乘积与反应物浓度幂指数乘积的比与K 大小。如果比K大,平衡向逆反应方向移动,V逆>V正;如果比K小,平衡向正反应方向移动, V正>V逆;如果等于K,平衡不会发生移动, V正=V逆;由于(0.6×0.6)/(0.4)2==9/4<400,所以平衡向正反应方向移动,V正>V逆。②化学平衡常数是可能反应达到化学平衡时隔生成物浓度幂指数的乘积与各反应物浓度幂指数的乘积的比即K={C(CH3OCH3)×C(H2O)} /C2(CH3OH).该反应的正反应是放热反应,升高温度,根据勒夏特列原理,化学平衡向逆反应方向移动,生成物的浓度减小,反应物的浓度增大,对化学平衡常数来说,分子减小,分母扩大,所以K减小。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源:不详 题型:实验题
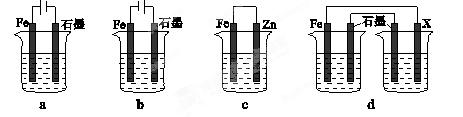
 2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1
2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1| | Fe2O3 | CO | Fe | CO2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
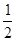 O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ①
O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ① O2(g)= HgO (s) △H= -Q2 kJ? mol-1 ②
O2(g)= HgO (s) △H= -Q2 kJ? mol-1 ②| A.Q2 -Q1 | B.Q1 +Q2 | C.Q1- Q2 | D.-Q1- Q2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g),写出该反应的化学平衡常数表达式:
2SO3(g),写出该反应的化学平衡常数表达式: 
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 SO3(g)+NO(g)将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
SO3(g)+NO(g)将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3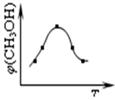
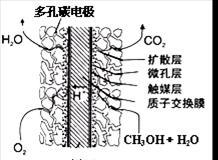
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
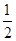 O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1| A.483.6 kJ | B.88 kJ | C.285.8 kJ | D.44 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 :的反应热ΔH为 ( )
:的反应热ΔH为 ( )| A.-1780kJ·mol-1 | B.-1220kJ·mol-1 | C.-450kJ·mol-1 | D.+430kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
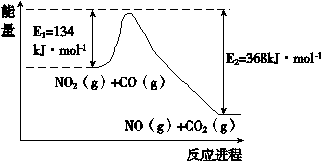
 2NH3 (g) ΔH<0,
2NH3 (g) ΔH<0,| T /K | 298 | 398 |
| 平衡常数K | K1 | K2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com