
【题目】查阅资料:元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)铬(24Cr)属于_______________(选填编号)。
a.主族元素 b.副族元素 c.Ⅷ族元素 d.过渡元素
(2)铬单质是银白色有金属光泽的固体,有较高的熔点,是最硬的金属;与Ni等添加到Fe中可制成不锈钢。比较硬度:纯铁_________不锈钢;熔点:纯铁__________不锈钢(填“>”“<”或“=”)。
(3)Cr(OH)3与Al(OH)3的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是___________________。
(4)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
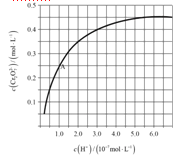
①用离子方程式表示Na2CrO4溶液中的转化反应____________________。
②由图可知,溶液酸性增大,CrO42的平衡转化率__________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH__________0(填“>”“<”或“=”)。
(5)+6价铬的化合物毒性较大,但其化合物用途广泛。如:“酒精检测仪”可检查司机是否酒驾,其反应原理为:m C2H5OH+ n X + p H2SO4═ g Cr2(SO4)3 + w CO2↑+ 9H2O,其中X的化学式最有可能为__________。常用NaHSO3将酸性废液中的Cr2O72还原成Cr3+,该反应的离子方程式为_______________。
【答案】
(1)bd(2)< >(各1分)
(3)蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解形成绿色溶液
(4)①2CrO42-+2H+![]() Cr2O72-+H2O② 增大 1.0×1014③小于
Cr2O72-+H2O② 增大 1.0×1014③小于
(5)CrO3 Cr2O72+3HSO3 +5H+=2Cr3++3SO42+4H2O
【解析】
试题分析:
(1)铬(24Cr)属于在周期表中第四周期ⅥB族,是副族元素,也是过渡元素,故选bd。
(2)合金比组成的金属熔点更低,但硬度等机械性能更高。故有纯铁的硬度小于不锈钢,纯铁的熔点高于不锈钢。
(3)Cr(OH)3与Al(OH)3的化学性质相似,可知Cr(OH)3是两性氧化物,能溶解在强碱NaOH溶液中,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,首先蓝紫色变浅同时产生Cr(OH)3灰蓝色固体,继续滴加,沉淀溶解,Cr(OH)3变为Cr(OH)4-,溶液最终变为绿色。故答案为:蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解形成绿色溶液。
(4)①随着H+浓度的增大,CrO42-与溶液中的H+发生反应,反应转化为Cr2O72-的离子反应式为:2CrO42-+2H+![]() Cr2O72-+H2O。②根据化学平衡移动原理,溶液酸性增大,c(H+)增大,化学平衡2CrO42-+2H+
Cr2O72-+H2O。②根据化学平衡移动原理,溶液酸性增大,c(H+)增大,化学平衡2CrO42-+2H+![]() Cr2O72-+H2O向正反应方向进行,导致CrO42的平衡转化率增大;根据图像可知,在A点时,c(Cr2O72-)=0.25 mol/L,由于开始时c(CrO42)=1.0 mol/L,根据Cr元素守恒可知A点的溶液中CrO42-的浓度c(CrO42)=0.5 mol/L;H+浓度为1.0×10-7 mol/L;此时该转化反应的平衡常数为
Cr2O72-+H2O向正反应方向进行,导致CrO42的平衡转化率增大;根据图像可知,在A点时,c(Cr2O72-)=0.25 mol/L,由于开始时c(CrO42)=1.0 mol/L,根据Cr元素守恒可知A点的溶液中CrO42-的浓度c(CrO42)=0.5 mol/L;H+浓度为1.0×10-7 mol/L;此时该转化反应的平衡常数为![]() ;③由于升高温度,溶液中CrO42的平衡转化率减小,说明升高温度,化学平衡逆向移动,导致溶液中CrO42的平衡转化率减小,根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应,故该反应的ΔH<0;
;③由于升高温度,溶液中CrO42的平衡转化率减小,说明升高温度,化学平衡逆向移动,导致溶液中CrO42的平衡转化率减小,根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应,故该反应的ΔH<0;
(5)根据原子守恒,可知X为CrO3。根据氧化还原反应原理可知,NaHSO3将酸性废液中的Cr2O72还原成Cr3+,该反应的离子方程式为Cr2O72+3HSO3 +5H+=2Cr3++3SO42+4H2O。


科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是

A. ①中溶液橙色加深,③中溶液变黄
B. ②中Cr2O72-被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性强
D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下。下列有关说法不正确的是( )

A. 制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO
B. 生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应
C. 粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D. 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”.试回答下列问题:
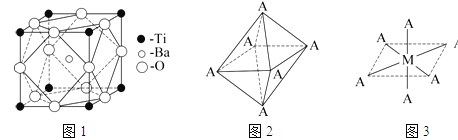
(1)Ti元素原子序数为22,它在元素周期表中的位置是第 周期第 族;其基态原子的电子排布式为 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定.偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图1所示,它的化学式是 ,其中Ti4+的氧配位数为 ,Ba2+的氧配位数为 。
(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点﹣23.2℃,沸点136.2℃,所以TiCl4应是
化合物,其固体是 晶体。TiCl4在潮湿空气中易挥发,水解而冒白烟,这是因为水解后有 生成。
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如图2所示,我们通常可以用图3所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有 种同分异构体,请将其结构画出_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。

⑴ Ⅰ中发生反应的化学方程式是 ,氧化剂与还原剂的物质的量之比是
⑵ Ⅱ中反应的离子方程式是
⑶ 装置Ⅲ中阳极的反应是 ;
⑷ ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
① 该反应中盐酸的作用是
② 写出实验室制氯气的离子方程式 ;说明上述两反应中盐酸作用不同的原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的泄漏会造成严重的危险,以下说法有科学性错误的是
A. 由于大量苯溶入水中,渗入土壤,会对周边农田、水源造成严重的污染
B. 由于苯是一种易挥发、易燃的物质,周围地区如果有火星就可能引起爆炸
C. 可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D. 由于苯有毒,所有工作人员在处理事故时,都要做相关防护措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学让生活更美好。以下说法错误的是( )
A.酒精溶液可以使蛋白质变性,酒精纯度越高杀菌消毒效果越好
B.在烟花中加入某些金属元素,使焰火更加绚丽多彩
C.苏打水呈弱碱性,可以舒缓胃酸分泌过多时的不适感
D.在葡萄酒中添加微量二氧化硫作抗氧化剂,使酒保持良好品质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为:Mg17Al12 + 17H2=17MgH2 + 12Al。得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。
⑴ 熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是
⑵ 在6.0 mol·L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17Al12 完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为
Ⅱ.某一反应体系有反应物和生成物共五种物质:
O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2―→O2
⑴ 该反应中的还原剂是
⑵ 该反应中,发生还原反应的过程是 →
⑶ 写出该反应的化学方程式,并标出电子转移的方向和数目 ;
⑷ 若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com