
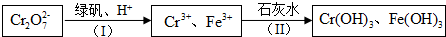
分析 (1)明矾中含有铝离子,易水解生成氢氧化铝胶体,胶体吸附水中的悬浮物而净水;
(2)混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒得c(OH-)=c(H+),据此确定溶液酸碱性,醋酸钠溶液呈碱性,要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠;
(3)室温下取0.2mol•L-1HCl溶液与0.2mol•L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=5,说明得到的盐是强酸弱碱盐;
(4)NaHA溶液中,HA-离子既电离也水解,测得溶液显碱性,说明其电离程
度小于水解程度;
(5)①依据氧化还原反应离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可以求得Cr2O72-与FeSO4的物质的量之比;
②据Ksp[Cr(OH)3]=6.0×10-31和c(Cr3+)=6.0×10-7 mol•L-1求得c(OH-)可求得pH.
解答 解:(1)明矾溶于水电离出铝离子,铝离子易水解生成氢氧化铝胶体,胶体具有吸附性,能吸附水中的悬浮物而净水,所以明矾能净水,离子方程式为Al3++3H2O?Al(OH)3+3H+,故答案为:Al3++3H2O?Al(OH)3+3H+;
(2)混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒得c(OH-)=c(H+),溶液呈中性,醋酸钠溶液呈碱性,要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠,醋酸和氢氧化钠浓度相等,所以醋酸体积大于氢氧化钠,
故答案为:大于;
(3)等体积等浓度的盐酸和MOH恰好反应生成盐,得到的盐溶液呈酸性,说明该盐是强酸弱碱盐,弱碱电离可逆,其电离方程式为:MOH?M++OH-,
故答案为:MOH?M++OH-;
(4)①NaHA溶液中,HA-离子既电离也水解,电离产生A2-,水解生成H2A,溶液显碱性,说明其电离程度小于水解程度,所以c(H2A)>c(A2-)故答案为:>;
②NaHA溶液中,HA-离子既电离也水解,电离产生A2-,水解生成H2A,溶液显碱性,说明其电离程度小于水解程度,
故答案为:NaHA溶液显碱性,说明其电离程度小于水解程度;
(5)①依据氧化还原反应离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可以求得Cr2O72-与FeSO4的物质的量之比为1:6,
故答案为:1:6;
②Ksp[Cr(OH)3]=c(Cr3+)c3(OH-)=c3(OH-)×6.0×10-7=6.0×10-31 ,c(OH-)=1.0×10-8 ,其pH=6,
故答案为:6.
点评 本题考查了盐类水解的应用、氧化还原反应计算应用,溶度积的计算应用等知识点,掌握基础是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
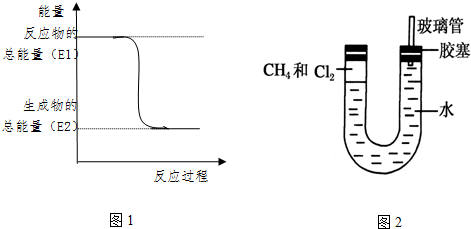
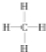 .一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.
.一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
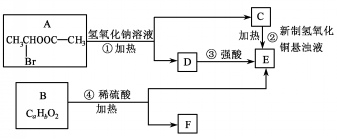
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、D2、T2互为同素异形体 | |
| B. | 液氨、氨水、王水都是混合物 | |
| C. | H2O、苯酚、Fe(SCN)3都是弱电解质 | |
| D. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
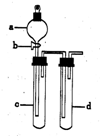 某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化.| 方 案 | 反 应 物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L氟化氢中含有分子的数目为0.5NA | |
| B. | 常温下a克某烷烃(CnH2n+2)中含有共用电子对数目为$\frac{a}{14n+2}$(3n+1)NA | |
| C. | 56g 聚乙烯中含有碳碳双键的数目为2NA | |
| D. | 常温下,0.2mol/L的FeCl3溶液中含Cl-数目为0.6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com