
| A. | 离子化合物中一定含有金属元素 | |
| B. | 只由共价键构成的物质不一定是共价化合物 | |
| C. | 原煤、天然气属于一次能源,而电力、蒸汽则属于二次能源 | |
| D. | 锌锰电池是一次电池,而铅蓄电池则是二次电池 |
分析 A.离子化合物中不一定含有金属元素,可能含有非金属元素氮元素和氢元素组成的铵根离子;
B.共价化合物中一定有共价键,离子化合物、非金属单质中也可能含有共价键;
C.一次能源是指直接取自自然界没有经过加工转换的各种能量和资源,由一次能源经过加工转换以后得到的能源产品,称为二次能源;
D.一次电池是放电后不能进行使用,二次电池是放电后可以充电后继续使用.
解答 解:A.离子化合物中不一定含有金属元素,如NH4NO3等铵盐,故A错误;
B.共价化合物中一定有共价键如HCl,含有共价键的物质可能为单质如氮气,离子化合物中可能含有共价键,如KOH,故B正确;
C.原煤、天然气是直接取自自然界没有经过加工转换的各种能量和资源,属于一次能源,而电力、蒸汽是由一次能源经过加工转换以后得到的能源产品,称为二次能源,故C正确;
D.碱性锌锰电池不能多次重复使用,属于一次电池;铅蓄电池能多次重复使用,属于二次电池,故D正确;
故选A.
点评 本题考查化学键、物质的分类,明确化学键和化合物的关系、一次电池、二次电池的工作实质是解本题关键,易错选项是B,注意离子化合物、非金属单质中也可能含有共价键为易错点.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Cu+O2═2 CuO | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 2KMnO4═K2MnO4+MnO2+O2↑ | D. | 2Na+2H2O═2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:5:2 | B. | 2:5:4 | C. | 1:3:2 | D. | 2:3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Cl2对自来水进行消毒杀菌 | |
| B. | 用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) | |
| C. | 用SO2漂白食品 | |
| D. | 用小苏打(NaHCO3)发酵面团制作馒头 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{n(m-x+2)}{m}$ mol | B. | $\frac{n(m-x)}{m}$ mol | C. | $\frac{m-x+2}{m-n}$ mol | D. | $\frac{n(m-x-2)}{m}$ mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | K+、Cu2+、SO42-、Cl- | ||
| C. | Na+、H+、Cl-、CO32- | D. | Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

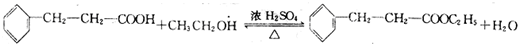 .
.
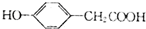 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g)
碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com