
【题目】下图为氢氧燃烧电池原理示意图,按照此图的提示,下列叙述正确的是( )
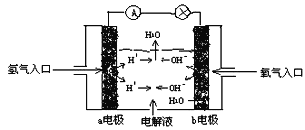
A. a电极是正极
B. b电极的电极反应为:4OH-- 4e-=2H2O + O2↑
C. 电子从a电极经由电解液传递到b电极
D. 氢氧燃烧电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知:①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) ΔH=-38.19 kJ·mol-1
则表示 CH3OH的燃烧热的热化学方程式为___________ 。
(2)在一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g) ![]() CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
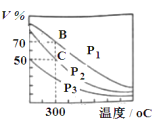
①该反应的反应热 ΔH________ 0(填“>”或“<”), 在_______ (填“高温”、“低温” )下易自发,压强的相对大小与 p1_______ p2(填“>”或“<”)。
②压强为 p2,温度为300℃时,该反应的化学平衡常数的计算表达式为 K=_______。
③下列各项中,不能说明该反应已经达到平衡的是_______。
A.容器内气体压强不再变化 B.υ(CO):υ(H2)=1:2
C.容器内的密度不在变化 D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证 H2浓度不变的情况下,增大容器的体积,平衡_______。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 有A、B、C三块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极;②A、C相连后,同时浸入稀H2SO4,C极发生氧化反应。则三种金属的活动性顺序为
A.A>C>B B.B>C>A C.C>A>B D.A>B>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2﹣甲基丙烷的一氯取代物有两种
B.![]() 和
和 ![]() 互为同系物
互为同系物
C.顺﹣2﹣丁烯与反﹣2﹣丁烯与氢气加成的产物不相同
D. 的名称为2﹣甲基﹣3﹣乙基丁烷
的名称为2﹣甲基﹣3﹣乙基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 一氧化二氮的摩尔质量是44 g B. 硫酸根的摩尔质量是96 g/mol
C. 1 mol O2的质量是32 g/mol D. 铁的摩尔质量就是铁的相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是( )
A. ![]() N2H4(g)+
N2H4(g)+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(g) ΔH=+267 kJ·mol-1
N2(g)+H2O(g) ΔH=+267 kJ·mol-1
B. N2H4(g)+O2(g)==N2(g)+2H2O(g) ΔH =-534 kJ·mol-1
C. N2H4(g)+O2(g)==N2(g)+2H2O(g) ΔH =+534 kJ·mol-1
D. N2H4(g)+O2(g)==N2(g)+2H2O(l) ΔH =-133.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.煤是由无机物和有机物共同组成的复杂混合物
B.红外光谱和紫外光谱可用来分析有机物结构
C.李比希提出基团的概念,并首次用无机物合成尿素,突破了有机物与无机物的界限
D.糖类、油脂、蛋白质是人类的重要营养物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年8月,四川九寨沟地震造成了重大人员财产损失。地震救援中需要使用大量的消毒剂,下列消毒剂属于强电解质的是
A. 次氯酸 B. 二氧化氯 C. 酒精 D. 高锰酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煅烧硫铁矿(主要成分为FeS2)的反应为:4FeS2+11O2 ![]() 2Fe2O3+8SO2 . 试回答下列问题.
2Fe2O3+8SO2 . 试回答下列问题.
(1)可用哪些物质来表示该反应的化学反应速率 .
(2)某时刻时测得,生成SO2的速率为0.64mol/(Ls),则氧气减少的速率为mol/(Ls).
(3)该工业生产中将矿石粉碎的目的: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com