
| A、沼气是一种清洁能源 |
| B、使用沼气级农民的生活带来了不便 |
| C、使用沼气作能源可以保护森林 |
| D、使用沼气是对化学能的充分利用 |
科目:高中化学 来源: 题型:
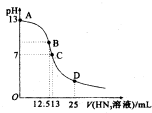 氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题:
氮气是空气中含量最多的一种气体,氮气及其化合物在工农业生产、生活中有着广泛的应用.请回答下列问题:| T(K) | 298 | 398 | 498 | … |
| K | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,有白色沉淀产生,说明蛋白质发生了变性 |
| B、棉花、纸、醋酸纤维的主要成分都是纤维素 |
| C、淀粉、牛油、蛋白质都是天然高分子化合物 |
| D、油脂里饱和烃基的相对含量越大,油脂的熔点越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2和O3互为同位素 |
| B、O2和O3的相互转化是物理变化 |
| C、在相同的温度与压强下,等体积的O2和O3含有相同的分子数 |
| D、等物质的量的O2和O3含有相同的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
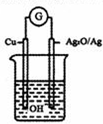 普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )| A、铜电极附近有黑色沉淀生成 |
| B、负极的电极反应式为2Cu+2OH--2e-═Cu2O+H2O |
| C、测量原理示意图中,电流方向从Cu经过导线流向Ag2O |
| D、电池工作时,溶液中OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28种 | B、32种 |
| C、40种 | D、48种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B、依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C、依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D、依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、A、B、D、E四种元素所形成的最高价含氧酸中D的酸性最强 |
| B、形成的简单阴离子半径的大小顺序为:C>B>D>E |
| C、D、E、F三种元素形成的单质中都含有共价键 |
| D、1 mo1A、B、C元素的简单氢化物中都含有10 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com