
(1)用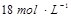 的硫酸配制
的硫酸配制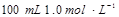 硫酸,若实验仪器有:
硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平
C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管
G.50mL烧杯 H.100mL容量瓶
实验时应选用仪器的先后顺序是(填入编号)_________________。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)___________________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线2cm~3cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近容量瓶刻度标线1cm~2cm处,用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
完成下列填空:
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1),应选用的仪器是 。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是 溶液,NaHCO3溶液可以吸收 。
(3)上述装置中,b物质是 。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果 (填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正已烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出 后溶出 。
(6)上述测定实验中,连续 ,说明样品已经恒重。
查看答案和解析>>
科目:高中化学 来源:2011—2012学年黑龙江哈九中度高二上学期期中考试化学试卷 题型:填空题
(10分)(1)写出稀硫酸与硫代硫酸钠溶液混合的离子方程式
(2)向FeCl3稀溶液中滴加少量KSCN稀溶液,离子方程式为
(2)若再向其中滴加少量硫氰化铵或硫酸铁浓溶液,现象是
(3)实验室配制FeCl3溶液的方法是:
(4)滴有酚酞试液的Na2CO3溶液显_______色,若给溶液加热,溶液颜色会_________,其原因是_____________________________________________(用方程式结合必要的文字回答)
查看答案和解析>>
科目:高中化学 来源:2010年广东省梅州市高三10月月考(理综)化学部分 题型:实验题
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
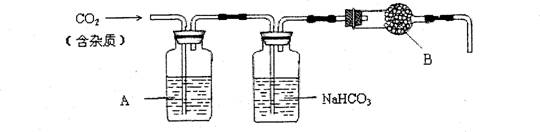
完成下列填空:
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1),应选用的仪器是 。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是 溶液,NaHCO3溶液可以吸收 。
(3)上述装置中,b物质是 。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果 (填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正已烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出 后溶出 。
(6)上述测定实验中,连续 ,说明样品已经恒重。
查看答案和解析>>
科目:高中化学 来源:2010年上海市高考化学试卷(解析版) 题型:解答题
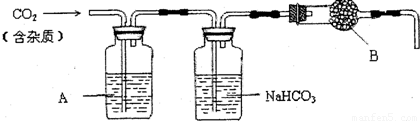
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com