
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图,下列说法错误的是

A.反应可表示为3X+Y![]() 2Z
2Z
B.从反应开始到0.4 s时,以Y表示的化学反应速率为0.25 mol·L-1·s-1
C.增大压强使平衡向生成Z的方向移动,正逆反应速率均增大
D.升高温度,平衡常数一定增大
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A. 图甲 中的ΔH1>ΔH2
中的ΔH1>ΔH2
B. 图乙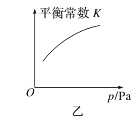 表示可逆反应A(s)+3B(g)2C(g) ΔH>0
表示可逆反应A(s)+3B(g)2C(g) ΔH>0
C. 图丙 表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
D. 由图丁 可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() ,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
,某研究小组将4moX和2molY置于一容积不变的密闭容器中,测定1min内X的转化率,得到的数据如表所示,下列判断正确的是( )
t/min | 2 | 4.5 | 5 | 6 |
X的转化率 | 30% | 40% | 70% | 70% |
A.随着反应的进行,混合气体的密度不断增大
B.反应在5.5min时,![]()
C.6min时,容器中剩余1.4molY
D.其他条件不变,将X的物质的量改为10mol,则可得到4molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
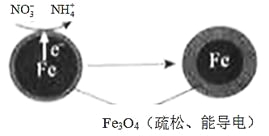
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3—的去除率低。其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3—的去除率。对Fe2+的作用提出两种假设:
Ⅰ. Fe2+直接还原NO3—;
Ⅱ. Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如右图所示,可得到的结论是_______。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高NO3—去除率的原因:______。
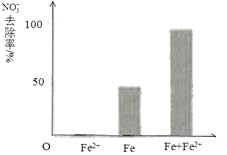
pH =4.5(其他条件相同)
(4)其他条件与(2)相同,经1小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3—去除率和铁的最终物质形态不同的原因:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:![]() 在恒温恒容密闭容器中反应,达到平衡状态的标志是
在恒温恒容密闭容器中反应,达到平衡状态的标志是
![]() 单位时间内生成n
单位时间内生成n![]() 的同时消耗2n
的同时消耗2n![]() ;
;
![]() 单位时间内生成n
单位时间内生成n![]() 的同时消耗2nmolNO;
的同时消耗2nmolNO;
![]() 混合气体的颜色不再改变的状态;
混合气体的颜色不再改变的状态;
![]() 混合气体中
混合气体中![]() 不变;
不变;
![]() 的消耗速率与NO的生成速率相等;
的消耗速率与NO的生成速率相等;
![]() 容器内压强不随时间变化而变化。
容器内压强不随时间变化而变化。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将0.1molAgCl固体加入1L0.1molL-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是( )
A.沉淀转化反应![]() 的平衡常数为20molL-1
的平衡常数为20molL-1
B.约有10-5molAgCl溶解
C.反应后溶液中的:c(Na+)>c(CO32-)>c(Cl-)>c(Ag+)>c(H+)
D.反应后溶液中的:c(Na+)+c(Ag+)=2c(CO32-)+c(HCO3-)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池总反应为4Al+3O2+6H2O=4Al(OH)3。下列说法不正确的是( )
A.正极的电极反应为O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大其与氧气的接触面积
D.该电池通常只需要更换铝板就可继续使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池,如图所示,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料产生能量。下列说法正确的是( )

A.a极为正极
B.随着反应的进行,负极区的pH不断增大
C.消耗0.1mol葡萄糖,电路中转移0.2mol电子
D.b极的电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com