
【题目】现有下列短周期元素的数据(已知Be的原子半径为0.089 nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高 正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低 负化合价 | -2 | -3 | -1 | -3 |
(1)⑧号元素在周期表中的位置是______________________________;表格中元素处于同一主族的是__________________________________。 (用元素符号表示)
(2)元素①和⑥能形成两种化合物,写出这两种化合物的电子式_______________________;________________________。
(3)④和⑤元素最高价氧化物对应的水化物酸性较强的是________(用物质化学式表示)。
【答案】第二周期ⅢA族 Li、Na 和N、P ![]()
![]() HClO4
HClO4
【解析】
元素①最低负价为-2价,且半径比Be原子小,则为O元素;元素②最高正价为+2价,应为第IIA族元素,半径比Be大,所以为Mg元素;③和⑥最高正价均为+1价,为第IA族元素,⑥的半径大于③,则③为Li,⑥为Na元素;④和⑦均为第ⅤA族元素,④半径较大,则④为P,⑦为N;⑤为Cl;⑧的最高正价为+3价,应为第IIIA族元素,其半径比Be小,则为B,以此来解答。
(1)⑧号元素为B,在周期表中的位置是第二周期第ⅢA族;上述元素处于同一主族的有Li、Na和N、P;
(2)①为O元素,⑥为Na元素,二者形成两种化合物:Na2O和Na2O2,两种化合物的电子式![]() 、
、![]() ;
;
(3)④为P,⑤为Cl,二者同周期,同周期元素随核电荷数增大,非金属性越强,非金属性越强,元素最高价氧化物对应水化物的酸性越强,Cl元素的非金属性强于P,则Cl元素最高价氧化物对应的水化物酸性较强,该酸是HClO4。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】美国康乃尔大学的魏考克斯(C·wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面上)。有关该有机分子的说法不正确的是( )

A. 属于芳香烃
B. 不属于苯的同系物
C. 分子中含有22个碳原子
D. 它和分子式为C22H12的有机物可能互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4-AFMF是一种探测物质的荧光素,其结构简式如下图。下列有关该物质的说法正确的是

A. 分子中三个苯环处于同一平面
B. 1 mol 4-AFMF 最多可与2molNaOH 反应
C. 在酸性条件下水解,水解产物只有1种
D. 能与溴水、FeCl3溶液及稀硫酸发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。
(1)已知25℃时:N2(g)+O2(g)![]() 2NO(g)△H=+183kJ/mol,2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ/mol,4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H=﹣1164.4kJ/mol,则N2(g)+3H2(g)
2NO(g)△H=+183kJ/mol,2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ/mol,4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H=﹣1164.4kJ/mol,则N2(g)+3H2(g)![]() 2NH3(g)△H=____________ ;
2NH3(g)△H=____________ ;
(2)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0mol/L | 3.0mol/L | 0 |
投料Ⅱ | 1.0mol/L | 2mol/L | 1.0mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡时化学平衡常数为0.1,则该温度下合成氨反应的平衡常数表达式为_____;
②按投料Ⅱ进行反应,起始时反应进行的方向为_____________(填“正向”或“逆向”);
③若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是____;
a.NH3是N2浓度的2倍b.容器中气体的压强不再改变c.2v(NH3)正=v(N2)逆d.容器中混合气体的密度不再改变e.容器中N2、H2、NH3物质的量之比为1:3:2f.混合气体平均相对分子质量保持不变
④若升高温度,则合成氨反应的化学平衡常数_______(填“变大”、“变小”或“不变”);
⑤L(L1、L2)、X可分别代表压强或温度。如图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系;

ⅰ)X代表的物理量是_________________;
ⅱ)判断L1、L2的大小关系,L1__________L2.(填“>”“<”或“=”)
⑶电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意如图:

①电极b上发生的是____________反应(填“氧化”或“还原”)。
②写出电极a的电极反应式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )

A.a处通入氧气,b处通入氢气
B.通入H2的电极发生反应:H2-2e-=2H+
C.通入O2的电极为电池的正极
D.该装置将化学能最终转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)画出下列各微粒的结构示意图:L层电子数为K、M层电子数之和的原子形成的阴离子________;与Ne原子电子层结构相同的+1价阳离子________。
(2)写出下列物质或离子的电子式
N2 ________CO2 _________ OH- ____________NH![]() ___________
___________
(3)用电子式表示H2S和MgBr2的形成过程
H2S ________________________________
MgF2_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“空气吹出法”海水提漠的工艺流程如下:
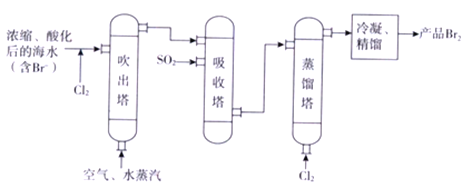
下列说法中,正确的是
A. 进入吹出塔前,Br -被还原成了Br2 B. 从吹出塔进入吸收塔的物质只有Br2
C. 经过吸收塔后,溴元素得到了富集 D. 蒸馏塔中只发生了物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】储氢纳米碳管的研究成功体现了科技的进步,但用电孤法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。反应化学方程式为:3C+2K2Cr2O7 +8H2SO4 = 3CO2↑+ 2K2SO4+2Cr2(SO4)3 +8 H2O
(1)上述反应中氧化剂是___________(填化学式), 被氧化的元素是_________(填元素符号)。
(2)H2SO4 在上述反应中表现出来的性质是____________(填选项编号)
A.氧化性 B.氧化性和酸性 C.还原性和酸性 D.酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为______________L。
(4)请用双线桥法标出电子转移的方向和数目___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molSO2和1molO2充入一定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-197kJ·mol-1,当达到化学平衡时,下列说法中正确的是
2SO3(g)ΔH=-197kJ·mol-1,当达到化学平衡时,下列说法中正确的是
A.v正(O2)=2v逆(SO2)B.SO2和SO3共2mol
C.放出197kJ热量D.SO2和O2浓度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com