
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:阅读理解
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+●提出假设: (1)假设①:该混合金属粉末中除镁外还含有 Al Al 元素假设②:该混合金属粉末中除镁外还含有 Zn Zn 元素假设③:该混合金属粉末中除镁外还含有铝、锌元素 ●实验探究: 甲同学基于假设③设计实验方案如下:乙同学同样基于假设③设计另一实验方案如下: 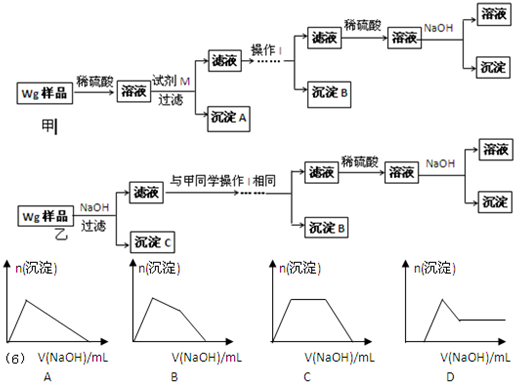 (2)试剂M是 NaOH溶液 NaOH溶液 ;沉淀B是Al(OH)3 Al(OH)3 .(3)丙同学认为乙同学的方案比甲同学的好,理由是 步骤简单,节约试剂 步骤简单,节约试剂 .(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是 将沉淀C洗涤、小心干燥后称量 将沉淀C洗涤、小心干燥后称量 .(5)操作Ⅰ的主要过程是:在滤液中逐滴加入 稀硫酸 稀硫酸 ,直至生成的沉淀刚好溶解,再加入足量的稀氨水 稀氨水 .(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图象正确的是 B B .
查看答案和解析>> 科目:高中化学 来源: 题型: 一定条件下铁可以和CO2发生反应: Fe(s)+CO2(g) (1)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,求8分钟内CO的平均反应速率v(CO)= 。 (2)下列措施中能使平衡时c(CO)/c(CO2)增大的是 (填序号)。 A.升高温度 B.增大压强 C.充入一定量氮气 D.再加入一些铁粉 (3)反应达到平衡后,若保持容器体积不变时,再通入一定量的CO2,则CO2的转化率将 (填“增大”、“减小”、“不变”),该反应的平衡常数K= ,温度升高,K (填“增大”、“减小”、“不变”)。 (4)铁的重要化合物在生产生活中应用十分广泛。高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂。高铁酸钠生产方法之一是:强碱性溶液中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和另一种常见化合物,该反应的离子方程式为 。 (5)已知:2CO(g)+O2(g)==2CO2(g)△H=-566 kJ/mol;2H2(g)+O2(g)==2H2O(g)△H=-483.6 kJ/mol。写出CO和H2O(g)作用生成CO2和H2的热化学方程式 。 (6)已知Ksp(Fe(OH)3)= 8´10-38,某溶液中含有Fe3的浓度是0.05mol×L-1。如果要使Fe(OH)3沉淀完全pH至少为 (溶液中离子浓度小于1×10-5mol/L时,沉淀完全,lg2=0.3)
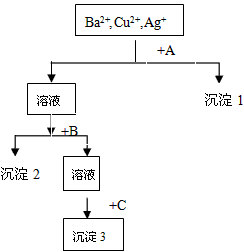
查看答案和解析>> 科目:高中化学 来源:2011-2012学年内蒙古呼伦贝尔市牙克石林业一中高一上学期期中考试化学试卷 题型:填空题 (10分)某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程如图(各步反应恰好完全进行) 查看答案和解析>> 科目:高中化学 来源:2010年宁夏高一上学期期中考试化学卷 题型:选择题 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如右图所示。下列说法正确的是( )
A.试剂A为Na2SO4溶液 B.沉淀3的化学式可能是BaSO4 C.生成沉淀1的离子方程式为:Cu2+ + 2OH- = Cu(OH)2↓ D.生成沉淀2的离子方程式为:Ag+ + Cl- = AgCl↓
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |