
| A、该弱酸溶液的pH=4 |
| B、加入NaOH溶液后,弱酸的电离平衡向右移动,但Ka不变 |
| C、加入等体积的0.01mol?L-1NaOH溶液后,所得的溶液的pH<7 |
| D、该弱酸的钠盐溶液一定会发生水解,常温下,其水解平衡常数Kh=10-8 |
| [H+]?[A-] |
| [HA] |
| [H+]?[A-] |
| [HA] |
| [OH-]?[HA] |
| [A-] |
| KW |
| Ka |
| 10-14 |
| 10-6 |


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
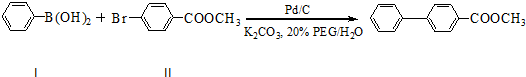

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 |
| B、某温度下,pH=6的蒸馏水显酸性 |
| C、氯气有毒,因而自来水的杀菌消毒一定不能使用氯气 |
| D、明矾可用于水的净化与杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 I--2e-=I2 碘遇淀粉变蓝 |
| B、Cu-2e-=Cu2+ Cu2+ 显蓝色 |
| C、2Cu+4I--4e-=2CuI↓+I2 碘遇淀粉变蓝 |
| D、4OH--4e-=2H2O+O2 O2将I-氧化为I2,碘遇淀粉变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
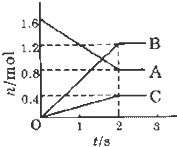 某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
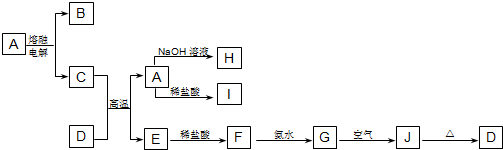
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com