
����Ŀ��ij��ѧ����С��Ϊ�ⶨ������CO2�ĺ���������������ʵ�飺
������0.1000 mol/L ��0.01000 mol/L�ı����ᡣ
�ڽ�2��3�η�̪����δ֪Ũ�ȵ�Ba(OH)2��Һ10.00 mL�У�����0.1000 mol/L�ı�������еζ��������ȥ����19.60 mL��
���òⶨ��Ba(OH)2��Һ���ն��������е�CO2��ȡBa(OH)2��Һ10.00 mL������100 mL����ƿ���ˮ���̶��ߣ�ȡ��ϡ�ͺ����Һ�����ܱ������ڣ���ͨ��10 L��״���µĿ���������ʱ���ɳ�����
�ܹ�������������Һ��
��ȡ��Һ20.00 mL����0.01000 mol/L������ζ�����ȥ����34.80 mL��
��ش��������⣺
��1�����Ʊ�����ʱ������������Щ����?_____________________��
A��������ƽ B������ƿ C����ʽ�ζ��� D����Ͳ E���ձ� F����ͷ�ι� G��������
��2���ڲ����е���ζ��յ�ʱ��������___________________________________________��
��3��Ba(OH)2��Һ�����ʵ���Ũ����________��
��4���˿�����Ʒ�к�CO2���������Ϊ________��
��5����ʵ���У�����һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������ע��ڶ��ֱ����ᣬ�����еڶ��εζ���ʹ�ⶨ���________(�ƫ��ƫС������Ӱ�족)��
��6���ڵ�һ�εζ���ʱ��δ��ϴ�ζ��ܣ���ʹ�ⶨ���_______(�ƫ��ƫС������Ӱ�족)��
���𰸡�B��D��E��F��G��Һ�ɺ�ɫǡ�ñ�Ϊ��ɫ���Ұ��������ɫ�ޱ仯0.09800 mol/L0.02500%ƫ��ƫ��
��������
(1)����һ�����ʵ���Ũ�ȵ�����ʱ�������м��㡢��ȡ��ϡ�͡�ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ�����ʵ�鲽������������ڽ�2��3�η�̪����δ֪Ũ�ȵ�Ba(OH)2��Һ����Һ�ʺ�ɫ����0.1000 mol/L�ı�������еζ����ζ��յ�ʱ��Һ��Ϊ��ɫ����3����������������������Ӧ�ķ���ʽ������Ba(OH)2��Һ�����ʵ���Ũ�ȣ���4�����ݻ�ѧ����ʽ���������Ʒ�к�CO2����������� (5) ��һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������ע��ڶ��ֱ����ᣬ�ڶ��εζ�����Ũ��ƫ���µڶ��εζ����ĵı�Һ�������ƫС��(6)������ʽ�ζ���û����ϴ�����µ�һ�εζ�����Ũ��ƫС�����ĵı�Һ�������ƫ���������������Ũ��ƫ��
(1)����һ�����ʵ���Ũ�ȵ�����ʱ�������м��㡢��ȡ��ϡ�͡�ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ���Ҫ������:����ƿ����Ͳ���ձ�����ͷ�ιܼ�����������BDEFG�� (2)��2��3�η�̪����δ֪Ũ�ȵ�Ba(OH)2��Һ����Һ�ʺ�ɫ����0.1000 mol/L�ı�������еζ�����Һ�ɺ�ɫǡ�ñ�Ϊ��ɫ���Ұ��������ɫ�ޱ仯���ﵽ�ζ��յ㣻(3)���ݷ�Ӧ����ʽ: Ba(OH)2+2HCl�TBaCl2+2H2O�� c[Ba(OH)2]��10.00mL=![]() ��0.1mol/L��19.60mL�����c[Ba(OH)2]=0.098mol/L�� (4)�����ķ�Ӧ����ʽ:Ba(OH)2+CO2�TBaCO3��+ H2O��20mL��Һ��Ba(OH)2�����ʵ���Ϊ34.80��10-3��0.01��
��0.1mol/L��19.60mL�����c[Ba(OH)2]=0.098mol/L�� (4)�����ķ�Ӧ����ʽ:Ba(OH)2+CO2�TBaCO3��+ H2O��20mL��Һ��Ba(OH)2�����ʵ���Ϊ34.80��10-3��0.01��![]() mol=0.174��10-3 mol��100mL��Һ�к��е��������������ʵ���Ϊ0.174��10-3��
mol=0.174��10-3 mol��100mL��Һ�к��е��������������ʵ���Ϊ0.174��10-3��![]() =8.70��10-4mol��ԭ�е��������������ʵ���Ϊ:0.098 mol/L��10��10-3L=9.8��10-4mol�������ж�����̼���ĵ��������������ʵ���Ϊ:9.8��10-4 mol-8.70��10-4 mol=1.1��10-4 mol��n(CO2)=n(Ba(OH)2)=1.1��10-4mol��������̼���������Ϊ:
=8.70��10-4mol��ԭ�е��������������ʵ���Ϊ:0.098 mol/L��10��10-3L=9.8��10-4mol�������ж�����̼���ĵ��������������ʵ���Ϊ:9.8��10-4 mol-8.70��10-4 mol=1.1��10-4 mol��n(CO2)=n(Ba(OH)2)=1.1��10-4mol��������̼���������Ϊ:![]() =0.025%��(5)��һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������ע��ڶ��ֱ����ᣬ���µڶ��εζ�����Ũ��ƫ�����ĵı�Һ�������ƫС�����������̼��Ӧ�������������ʵ���ƫ������ƫ��
=0.025%��(5)��һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������ע��ڶ��ֱ����ᣬ���µڶ��εζ�����Ũ��ƫ�����ĵı�Һ�������ƫС�����������̼��Ӧ�������������ʵ���ƫ������ƫ��
(6)������ʽ�ζ���û����ϴ�����µ�һ�εζ�����Ũ��ƫС�����ĵı�Һ�������ƫ���������������Ũ��ƫ�����������̼��Ӧ�������������ʵ���ƫ������ƫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦmX(g)+nY(g)![]() qZ(g)����H < 0,m+n>q,�ں����ܱ������з�Ӧ�ﵽƽ��ʱ������˵����ȷ����
qZ(g)����H < 0,m+n>q,�ں����ܱ������з�Ӧ�ﵽƽ��ʱ������˵����ȷ����
A. ͨ��ϡ������ʹѹǿ����ƽ�⽫�����ƶ�
B. X������Ӧ������Y���淴Ӧ���ʵ�n/m��
C. ����X�����ʵ�����Y��ת���ʽ���
D. �����¶ȣ���������ƽ����Է����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����Һ��c(H��)��0.1 mol��L��1�������Һ�����ʵ���Ũ��(����)
A.һ������0.1 mol��L��1B.һ������0.1 mol��L��1
C.һ��С��0.1 mol��L��1D.��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������仯ʾ��ͼ�������Ȼ�ѧ����ʽ��ȷ����

A. 2A��g��+ B(g)=2C��g����H=a��a��0��B. 2A��g��+ B(g)=2C��g����H=a��a��0��
C. 2A + B=2 C��H=a��a��0��D. 2C=2A +B��H=a��a��0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ƶ�ʵ�鷽���ܴﵽ��Ӧʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
A | ̽����ѧ��Ӧ���� | ȡ5mL0.1mol/LKI��Һ,�μ�0.1molLFeCl3��Һ5��6�Σ���ַ�Ӧ���ɸ�����Һ�мȺ�I2�ֺ�I-��ʵ����ʵ�жϸ÷�Ӧ�ǿ��淴Ӧ |
B | ̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�� | ����֧�Թܸ�ȡ5ml.0.1mo/L��KMnO4��Һ���ֱ����2mL0.1mol/L��10.2mol/L��H2C2O4(����)��Һ����¼��Һ��ɫ�����ʱ�� |
C | ֤�������к��е�Ԫ�� | ���������顢������ˮ���ݣ�ȡ��Һ�Ӽ���ϡ�����1mLH2O2���ټ��뼸�ε�����Һ����Һ���� |
D | ��֤CH3COONa ��Һ�д���ˮ��ƽ�� | ȡCH3COONa��Һ���Թ��в����뼸�η�̪�Լ����ټ������粒���(��ˮ��Һ������)���۲���Һ��ɫ�仯 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е�ʵ�����������������������
A.��25 mL�ļ�ʽ�ζ�����ȡ14.80 mL NaOH��Һ
B.��100 mL��Ͳ��ȡ5.2 mL����
C.��������ƽ��ȡ25.20 g�Ȼ���
D.��150 mL����ƿ����50 mL 0.1 mol/L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 500�桢30MPa������0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ�����Ȼ�ѧ����ʽΪ��N2(g)��3H2(g)![]() 2NH3(g) ��H=��38.6kJ��mol��1
2NH3(g) ��H=��38.6kJ��mol��1
B. �����ȼ����Ϊ-890.3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H= ��890.3kJ��mol-1
C. ԭ����з����ķ�Ӧ�ﵽƽ��ʱ���õ�����е�������
D. 500 mL 2.0 mol��L-1��HCl(aq)��500 mL 2.0 mol��L-1��NaOH(aq)��Ӧ����������������57.3 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ڱ������ˮϡ�͵Ĺ����У���Һ�ĵ���������I�����ż���ˮ�����V�仯��������ͼ��ʾ������˵����ȷ������ ��
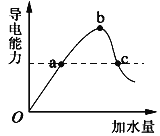
A��a��c����pH��ͬ
B����c��Һ�м�ˮ����Һ����������Ũ�ȶ���С
C������ʪ���pH��ֽ��b��pH���ƫ��
D��![]() b�����c��
b�����c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհס�
(1)�ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��______________��ֱ�������һ���������Һ��________ɫ��Ϊ________ɫ����________Ϊֹ��
(2)���в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���__________��
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
(3)ijѧ������3��ʵ��ֱ��¼�й��������±���
�ζ� ���� | ����NaOH ��Һ�����/mL | 0.100 0 mol��L��1 ��������/mL | ||
�ζ�ǰ���� | �ζ������ | ��Һ���/mL | ||
��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
������ | 25.00 | 0.22 | 26.31 | 26.09 |
�����ϱ����ݼ����NaOH��Һ�����ʵ���Ũ��___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com