
| A. | CO2+H2O═H2CO3 | B. | NH4HCO3═CO2↑+H2O+NH3↑ | ||
| C. | Zn+H2SO4═H2↑+ZnSO4 | D. | Cu(OH)2+2HCl═CuCl2+2H2O |
科目:高中化学 来源: 题型:解答题
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与等物质的量稀硫酸混合:Ba2++2OH-+2H++SO42-═BaSO4↓+2 H2O | |
| B. | 少量CO2通入澄清石灰水中:Ca(OH)2+CO2═CaCO3↓+H2O | |
| C. | 铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag | |
| D. | 碳酸钡溶于稀盐酸中:BaCO3+2H+═Ba2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
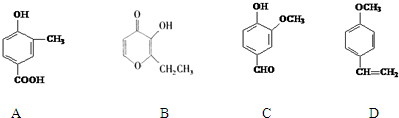
 ;
;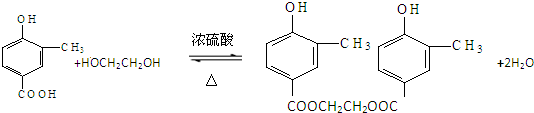 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;写成B与足量NaHCO3溶液完全反应的化学方程式:
;写成B与足量NaHCO3溶液完全反应的化学方程式: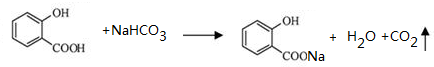 .
. .
. )是一种重要的有机合成中间体.根据图中提示的信息,试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).
)是一种重要的有机合成中间体.根据图中提示的信息,试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1用于放出碘的四氯化碳溶液 | |
| B. | 图2用于实验室收集SO2 | |
| C. | 图3用于实验室制备Fe(OH)2 | |
| D. | 图4用于比较NaHCO3和Na2CO3热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,将pH=11的氢氧化钠溶液稀释100倍后,溶液的pH=13 | |
| B. | pH=1的盐酸和醋酸溶液,分别加水稀释100倍后醋酸溶液pH更小 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,醋酸溶液消耗NaOH的物质的量更多 | |
| D. | pH=1的洁厕剂中c(H+)是pH=6的洗发液中c(H+)的105倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com