
| A. | 单质硅是将太阳能转变为电能的常用材料 | |
| B. | SiO2与酸、碱均不反应 | |
| C. | 因为SiO2有导电性,故SiO2可用于制备光导纤维 | |
| D. | 向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明H2SiO3的酸性比H2CO3的酸性强 |
分析 A、单质硅可用于制作太阳能电池的原料;
B、二氧化硅是酸性氧化物;
C、二氧化硅不导电,是制光导纤维的原料;
D、强酸制弱酸.
解答 解:A、单质硅可用于制作太阳能电池的原料,太阳能电池可将太阳能转化为电能,故A正确;
B、二氧化硅是酸性氧化物与碱反应生成盐和水,故B错误;
C、二氧化硅不导电,是制光导纤维的原料,故C错误;
D、向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明生成硅酸,根据强酸制弱酸,所以H2SiO3的酸性比H2CO3的酸性弱,故D错误;
故选A.
点评 本题考查化学与生活,为高频考点,涉及硅及其化合物性质等知识点,侧重考查基本概念及基本性质,明确物质性质和用途关系,题目难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| A. | Q1<Q2 | |
| B. | △H1能表示单质碳的标准燃烧热 | |
| C. | 生成物总能量均低于反应物总能量 | |
| D. | 1molCO2气体具有的能量大于1mol干冰具有的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;V\;}}{\;}$Fe(OH)3↓+3H+ | |
| C. | 实验室盛装NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| D. | 向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 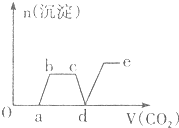 | ||
| C. | 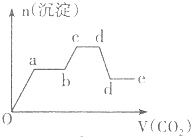 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2和氯水有漂白性 | 两者都能使溴水褪色 |
| B | CuSO4可以用作游泳池消毒剂 | 铜盐能使蛋白质变性 |
| C | 盐酸和氨水能溶解Al(OH)3 | Al(OH)3是两性氢氧化物 |
| D | 浓H2SO4可干燥CO和SO2 | CO和SO2都有较强的还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向H2SO4溶液中加入Ba(OH)2溶液 | B. | 向AlCl3溶液中通入氨气 | ||
| C. | 向Na2S溶液中通入SO2 | D. | 向Fe2(SO4)3溶液中加入Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe$\stackrel{盐酸}{→}$FeCl3$\stackrel{Fe}{→}$FeCl2 | |
| B. | Al(OH)3$\stackrel{盐酸}{→}$AlCl3(aq)$\stackrel{蒸发}{→}$无水AlCl3 | |
| C. | NH4Cl(s)$→_{△}^{Ca(OH)_{2}(s)}$NH3$\stackrel{MgCl(aq)}{→}$Mg(OH)2) | |
| D. | C6H5ONa$\stackrel{盐酸}{→}$C6H5OH$\stackrel{Na_{2}CO_{3}(aq)}{→}$CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于10s | B. | 等于10s | C. | 大于10s | D. | 等于5s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com