
| A. | 被浓NaOH溶液灼伤后,先用大量水冲洗,再用醋酸溶液冲洗 | |
| B. | 因吸入溴蒸汽而引起中毒时,可吸入适量的乙醇和乙醚的混和气体解毒 | |
| C. | 皮肤沾有苯酚时,立即用乙醇擦洗 | |
| D. | 吸入了一氧化碳而有中毒症状,赶快到空气新鲜且流通的地方 |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
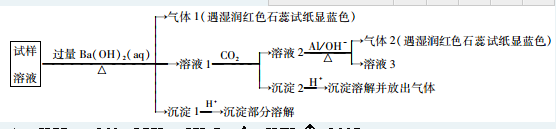

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同周期元素的原子电子层数相同 | |
| B. | (长式)元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| C. | 最外层电子数相同的元素都是同一族的元素 | |
| D. | 同一主族元素的原子最外层电子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 或
或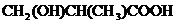 或
或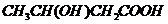 或
或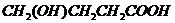


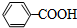
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
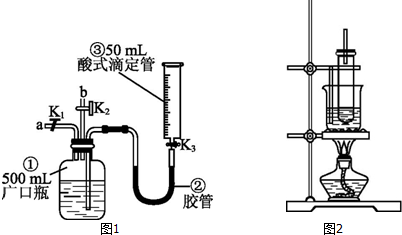
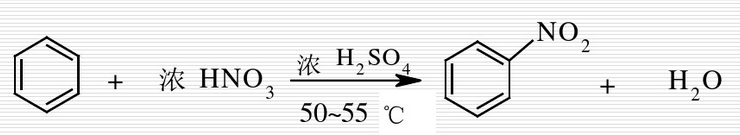 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述I | 叙述II |
| A | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙烯可与KMnO4溶液发生反应 | 乙烯具有还原性 |
| D | 乙醇的沸点比乙酸的沸点高 | 乙醇和乙酸可通过蒸馏初步分离 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com