
| A�� | 0.1 mol/LCH3COOH��Һ�У�c��CH3COO-��+c��CH3COOH��=0.1mol/L | |
| B�� | ��0.2 mol/L NaA��Һ��0.1 mol/L��������������ü�����Һ�У�c��Na+��+c��H+��=c��A-��+c��Cl-�� | |
| C�� | CH3COONa��Һ�У�c��Na+����c��CH3COO-����c��OH-����c��H+�� | |
| D�� | Na2S��Һ�У�c��Na+��=2��c��S2-��+c��HS-��+c��H2S���� |
���� A.0.1 mol/LCH3COOH��Һ�д��������غ㣻
B����0.2 mol/L NaA��Һ��0.1 mol/L����������ϵõ���Ũ�ȵ�NaCl��NaA��HA�Ļ����Һ����Һ�д��ڵ���غ��жϣ�
C����������Һ�д��������ˮ����Һ�Լ��ԣ�
D��Na2S��Һ�д��������غ�n��Na��=2n��S����
��� �⣺A.0.1 mol/LCH3COOH��Һ�д��������غ㣺c��CH3COO-��+c��CH3COOH��=0.1mol/L����A��ȷ��
B����0.2 mol/L NaA��Һ��0.1 mol/L����������ϵõ���Ũ�ȵ�NaCl��NaA��HA�Ļ����Һ����Һ�д��ڵ���غ�c��Na+��+c��H+��=c��A-��+c��Cl-��+c��OH-������B����
C��CH3COONa��Һ�д��������ˮ����Һ�Լ��ԣ�����Ũ�ȴ�С��c��Na+����c��CH3COO-����c��OH-����c��H+������C��ȷ��
D��Na2S��Һ�д��������غ�n��Na��=2n��S����c��Na+��=2��c��S2-��+c��HS-��+c��H2S��������D��ȷ��
��ѡB��
���� ���⿼���˵������Һ������Ũ�ȴ�С������غ㡢�����غ�����жϣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ԭ�� | N | S | O | Si |
| �뾶r/10-10 m | 0.75 | 1.02 | 0.73 | 1.11 |
| A�� | 1.10��10-10 m | B�� | 0.80��10-10 m | C�� | 0.70��10-10 m | D�� | 1.20��10-10 m |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{\;}^{12}$C��14C | B�� | ������Һ�� | C�� | ��������춡�� | D�� | ���Ͱ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��λʱ�������� n molA2��ͬʱ���� 2n molAB | |
| B�� | ��λʱ�������� n molABͬʱ���� n molB2 | |
| C�� | ��λʱ�������� n molA2ͬʱ���� n molB2 | |
| D�� | �����ڵ�����ƽ��Ħ����������ʱ��ı仯���仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ֱ��ˮϡ��100����������Һ��pH�仯�ȴ�����ҺС | |
| B�� | ������Һ�У���ˮ�������c��H+��=1��10-11mol•L-1 | |
| C�� | ��pH=11��NaOH��Һ�������Ϻ�ǡ���к� | |
| D�� | �ֱ��������пƬ��ַ�Ӧ������Һ�в���������һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
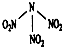 ��ѧ��������Ƴ�������Ϊ��Ч����ƽ�����N��NO2��3����ͼ��ʾ������֪�÷�����N-N-N���Ƕ���108.1�㣬�����й�N��NO2��3��˵����ȷ���ǣ�������
��ѧ��������Ƴ�������Ϊ��Ч����ƽ�����N��NO2��3����ͼ��ʾ������֪�÷�����N-N-N���Ƕ���108.1�㣬�����й�N��NO2��3��˵����ȷ���ǣ�������| A�� | ������N��O���γɵĹ��ۼ��ǷǼ��Լ� | |
| B�� | �������ĸ���ԭ�ӹ�ƽ�� | |
| C�� | �����ʼ������������л�ԭ�� | |
| D�� | 15.2g�����ʺ���6.02��1022��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ŨH2SO4����ˮ�ԣ������������� | |
| B�� | �����£�ŨH2SO4���������ܱ��������� | |
| C�� | ŨH2SO4���������ԣ�ϡH2SO4�������� | |
| D�� | ŨH2SO4�ѻӷ���������ڳ��������д��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
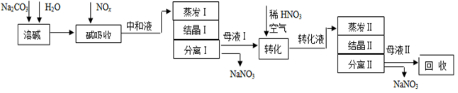
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com