
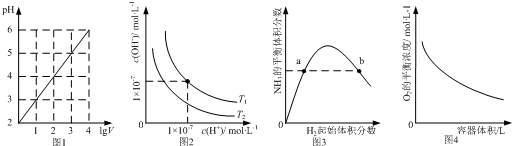
| A�� | ͼ1��ʾ1 LpH=2��CH3COOH��Һ��ˮϡ����V L��pH��lgV�ı仯 | |
| B�� | ͼ2��ʾ��ͬ�¶���ˮ��Һ��H+��OH-Ũ�ȵı仯�����ߣ�ͼ���¶�T2��T1 | |
| C�� | ͼ3��ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ���������N2����ʼ���㶨���ı仯��ͼ��a��N2��ת����С��b�� | |
| D�� | ͼ4��ʾͬһ�¶��£��ڲ�ͬ�ݻ��������н��з�Ӧ2BaO2��s��?2BaO��s��+O2��g����O2��ƽ��Ũ���������ݻ��Ĺ�ϵ |
���� A����ˮϡ��10n�����ٽ�����ĵ��룬��Һ��pH�仯С��n����λ��
B�����´ٽ�ˮ���룬Kw����
C������������Ũ�ȣ���ߵ�����ת���ʣ�
D��ƽ�ⳣ��k=c��O2��ֻ���¶��йأ�
��� �⣺A����ˮϡ��10n�����ٽ�����ĵ��룬��Һ��pH�仯С��n����λ������1 LpH=2��CH3COOH��Һ��ˮϡ����V L��pH�仯С��lgV����A����
B�����´ٽ�ˮ���룬Kw����ˮ�����������Ũ����������������Ũ�ȴ���¶ȸߣ����¶�T2��T1����B����
C������������Ũ�ȣ���ߵ�����ת���ʣ�������H2��ʼ�����������N2��ת��������a��N2��ת����С��b�㣬��C��ȷ��
D��2BaO2��s��?2BaO��s��+O2��g���÷�Ӧ��ƽ�ⳣ��k=c��O2��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣬����ͬһ�¶��£�c��O2�����䣬ͼ������D����
��ѡC��
���� ���⿼��������ĵ��롢Ӱ��ˮ�ĵ���ƽ������ء���ѧƽ���ƶ��ȣ���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������ע������йصķ�Ӧԭ���Լ�Ӱ��ƽ���������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 60g�����������Ҵ�����������Ӧ����ַ�Ӧ����ѵ�C-O����ĿΪNA | |
| B�� | ��������1LpH=1�Ĵ�����Һ�м�ˮ��������Һ��H+��Ŀ����0.1NA | |
| C�� | ij��ˮ�Ҵ������������Ʒ�Ӧ����5.6LH2�����Ҵ������й��ۼ�����Ϊ4NA | |
| D�� | ��֪C2H4��g��+H2��g��=C2H4��g����H=-137.0kJ/mol����ϩ��H2�ӳ�ʱ�ų�68.5kJ��������Ӧ�����б��ƻ���̼ԭ��֮�乲�õ��Ӷ���ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�������Ӻ�һ�������� | B�� | һ�ֵ��ʷ��Ӻ�һ�ֻ�������� | ||
| C�� | ����ԭ�� | D�� | һ��ԭ�Ӻ�һ�ַ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 1 | �� | �� | ||||||
| 2 | �� | �� | �� | �� | �� | |||
| 3 | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ԭ�ӷ��ţ�H | B�� | H2O2���ӽṹʽ��H-O-O-H | ||
| C�� | Mg2+�ṹʾ��ͼ��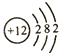 | D�� | HF���γɹ��� 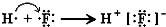 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba2+��Na+��OH-��SO42- | B�� | H+��Na+��I-��Cl- | ||
| C�� | HCO3-��K+��NO3-��OH- | D�� | H+��Fe2+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Իش�
�Իش� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
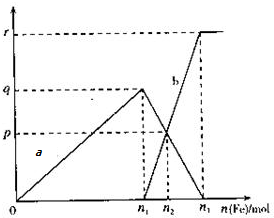 ��11.2mol/L��ϡ������Һ���������ۣ���Ӧ��������������ʵ������������۵����ʵ����Ĺ�ϵ��ͼ��ʾ������������Ϊ������������ʵ�����������Ϊ�������۵����ʵ���������ش��������⣺
��11.2mol/L��ϡ������Һ���������ۣ���Ӧ��������������ʵ������������۵����ʵ����Ĺ�ϵ��ͼ��ʾ������������Ϊ������������ʵ�����������Ϊ�������۵����ʵ���������ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com