
��7�֣�Ϊ���о���������Թ�������ֽ����ʵ�Ӱ�죬ijͬѧ��������ʵ�飺
| ��� | ���� | ʵ������ |
| �� | �ֱ����Թ�A��B�м���5 mL 5% H2O2��Һ��������2��1 mol��L��1 FeCl3��Һ�����Թ��о����������ݳ���ʱ�����Թ�A����ʢ��5��������ˮ���ձ��н��ݣ����Թ�B����ʢ��40��������ˮ���ձ��н��� | �Թ�A�����������ݲ����� �Թ�B�в��������������� |
| �� | ��ȡ��֧�Թֱܷ����5 mL 5% H2O2��Һ��5 mL 10% H2O2��Һ | �Թ�A��B�о�δ���Լ��������ݲ��� |
��1��2H2O2  2H2O+O2����1�֣� ��2���о��¶ȶ�H2O2�ֽ����ʵ�Ӱ�죨1�֣�
2H2O+O2����1�֣� ��2���о��¶ȶ�H2O2�ֽ����ʵ�Ӱ�죨1�֣�
��Ϊ�������ӿ�H2O2�ֽ����� ��1�֣�
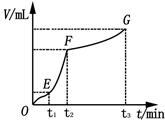
��3������֧�Թ�ͬʱ����ʢ����ͬ�¶���ˮ���ձ��У�������֧�Թ���ͬʱ����2��1mol��L��1 FeCl3��Һ�����۲�������ݵ����ʣ�2�֣� ��4��EF��2�֣�
���������������1����������ֽ⣬���������ڴ˷�Ӧ����������������ã��ܼӿ��������ֽ�������������ʣ��ʴ�Ϊ��2H2O2  2H2O+O2����
2H2O+O2����
��2���ֱ����Թ�A��B�м��� 5mL 5% H2O2��Һ��������1��2 ��1mol/L FeCl3��Һ�����Թ��о����������ݳ��֣�˵����������ֽ��ܷ������Թ�A��B�о����������ݳ���ʱ�����Թ�A����ʢ��5��������ˮ���ձ��У����Թ�B����ʢ��40��������ˮ���ձ��У���֧�Թܲ�ͬ�����Թ�A���¶ȱ��Թ�B���¶ȵͣ�˵���о������¶ȶԷ�Ӧ���ʵ�Ӱ�죬����ʼ�ӵμ�FeCl3��Һ��Ŀ�ļӿ�H2O2�ֽ⣬�ʴ�Ϊ���о��¶ȶ�H2O2�ֽ����ʵ�Ӱ�죻�ӿ�H2O2�ֽ����ʣ�ʹʵ���������ڹ۲죻
��3��Ӱ�컯ѧ��Ӧ���ʵ����������Ũ�ȡ��¶ȡ������ѹǿ������������ı��������ȡ��֧�Թֱܷ���� 5mL 5%H2O2��Һ�� 5mL10%H2O2��Һ���Թ�A��B�о�δ�����ݲ�����Ϊ�ӿ췴Ӧ���ʣ��ɴ��¶ȡ��������Ӱ��Ƕȿ��ǣ��ʴ�Ϊ������֧�Թ�ͬʱ����ʢ����ͬ�¶���ˮ���ձ��У�������֧�Թ���ͬʱ����2��1mol/L FeCl3��Һ���۲�������ݵ����ʣ�
��4����ͼ��������ʾʱ�䣬�������ʾ��������������ʱ��Խ�����ɵ�����Խ�࣬��Ӧ����Խ�죬���ߵ�б��Խ����������������EF�Ρ�
���㣺������������Է�Ӧ���ʵ�Ӱ���Լ�ѧ����ʵ��̽������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��8�֣���200mL 6mol��L-1�����м���һ�����Ĵ���CaCO3����������������ʱ��ı仯������ͼ��ʾ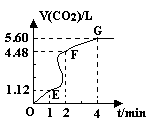 ������������ڱ�״���²ⶨ������ش��������⣺
������������ڱ�״���²ⶨ������ش��������⣺
��1����OE�εķ�Ӧ����Ϊv1��EF�εķ�Ӧ����Ϊv2��
FG�εķ�Ӧ����Ϊv3���� Ӱ��v1��v2��v3��Ӧ���ʵ������� ��
��2��Ϊ�˼���������Ӧ�����ʣ��������Һ�м����������ʣ�����Ϊ���е��� ������ĸ��
| A������ˮ | B���Ȼ��ع��� | C���Ȼ�����Һ | D��Ũ���� |
 ��3������CaCO3������Ϊ ��
��3������CaCO3������Ϊ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��ҵ������Ϊԭ��(����Ͻ���Ϊ����)��������������Ĺ������£�
|

 ��1����֪��Ӧһ������������Ͻ����ͻᴦ�ں���״̬��д�����������Ļ�ѧ����ʽ��______________________________________________�����¶�����ʱ���÷�Ӧ��ƽ�ⳣ��Kֵ___________(���������С�����䡱)��
��1����֪��Ӧһ������������Ͻ����ͻᴦ�ں���״̬��д�����������Ļ�ѧ����ʽ��______________________________________________�����¶�����ʱ���÷�Ӧ��ƽ�ⳣ��Kֵ___________(���������С�����䡱)�� 2NH3���÷�Ӧ�ڹ̶��ݻ����ܱ������н��С����и����־�Ÿ÷�Ӧ�ﵽ��ѧƽ��״̬����____________(�����)
2NH3���÷�Ӧ�ڹ̶��ݻ����ܱ������н��С����и����־�Ÿ÷�Ӧ�ﵽ��ѧƽ��״̬����____________(�����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
����β���к���CO��NO2���ж����壬��������װβ������װ�ã���ʹ�ж��������Ӧת��Ϊ�����塣
��1������β����CO��NO2������һ�������¿��Է�����Ӧ��
4CO(g)+2NO2(g) 4CO2(g)+N2(g)����H=��1200 kJ��mol��1
4CO2(g)+N2(g)����H=��1200 kJ��mol��1
�ٺ��º��������£�����˵���÷�Ӧ�Ѵﵽƽ��״̬����________(�����)��
A�������ڻ��������ɫ���ٱ仯 B�������ڵ�ѹǿ���ֲ���
C��2v��(NO2)=v��(N2) D�������ڻ�������ܶȱ��ֲ���
����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ�����淴Ӧ�����ƶ�����________(�����)��
A����ʱ�����CO2 B���ʵ������¶�
C����С�������ʹ��ϵѹǿ���� D��ѡ���Ч����
�۶��ڸ÷�Ӧ���¶Ȳ�ͬ(T2>T1)������������ͬʱ������ͼ����ȷ����________(�����)��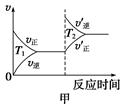
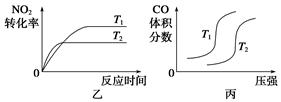
��2������β����CO��H2O(g)��һ�������¿��Է�����Ӧ��CO(g)+H2O(g) CO2(g)+H2(g) ��H<0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����ұ�����Ͷ�ϣ��ﵽƽ��״̬ʱK=1.0��
CO2(g)+H2(g) ��H<0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����ұ�����Ͷ�ϣ��ﵽƽ��״̬ʱK=1.0��
| ��ʼ���ʵ��� | �� | �� | �� |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��ͼΪ��ȡ����������ʵ��װ��ͼ���ش��������⣺ 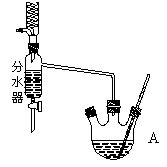
��ʾʵ��ԭ��
�������Ҵ��ڴ������ڵ������¼��ȿ��Է�����Ӧ��������������������ͬλ��ʾ�ٷ�д���������Ҵ�����������Ӧ�Ļ�ѧ����ʽ______________________��
�ܷ�����ͬλ��ʾ�ٷ���ʾ������Ӧԭ���� _______��ѡ��ܡ����ܡ�����ԭ����___________________��
��Ӧ�¶�ȷ����
�ϳ����������ķ�ӦΪ���ȷ�Ӧ��ʵ���������Ӧ�¶�Ӧ������85������Ϊ�ˡ��ش�
ʵ���¶Ȳ��˵���85�����ҵ�ԭ����__________________________________________��
ʵ���¶Ȳ��˸���85�����ҵ�ԭ����__________________________________________��
ʵ��װ�õıȽϣ�
������ͼװ���Ʊ���������������װ����̲�װ����Ƚ�ͻ�����ŵ���___________��
�����ȵı�ʾ��
Ϊ���õزⶨ�����ȣ���Ԥ����Na2CO3��Һ�еμ�1��____��Һ��������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ij̽��С���ý������ֱ���ϡ�����ϡ���ᷴӦ�ķ����о������벻ͬ�ᷴӦ�IJ��켰Ӱ�췴Ӧ�ٶȵ����ء�
ʵ��ҩƷ��2.0 mol/L���ᡢ4.0 mol/L���ᡢ2.0 mol/L���ᡢ4.0 mol/L���ᡢ��ͬ��С����Ƭ������(������������Ĥ���ѳ�ȥ)��ÿ��ʵ��������������Ϊ50.0 mL������������Ϊ9.0 g��
��.��ͬѧ����Ƭ�ֱ��ϡ���ᡢϡ���ᷴӦ��ʵ�鼰���������£�
| ��Ӧ���� (����) | 1 | 2 | 5 | 15 | 20 |
| 4.0 mol/L ���� | �������� | �϶����� | �������� | ��Ӧ���� | ��Ƭ�ľ� |
| 2.0 mol/L ���� | ���������� | ������ ���� | �������� | ||
| 4.0 mol/L ���� | ���������� | �������� | �бȽ����������� | ||
| ʵ��Ŀ�� | ʵ�� ��� | �¶� /�� | �������� ��̬ | ����Ũ�� /mol��L��1 |
| 1.ʵ��ٺ͢�̽������Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻 2��ʵ��ٺ͢�̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻 3��ʵ��ٺ͢�̽���������(��Ƭ�� ����)�Ը÷�Ӧ���ʵ�Ӱ�� | �� | 25 | ��Ƭ | 4.0 |
| �� | | | | |
| �� | | | | |
| �� | | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��14�� ÿ��2�֣�����ԭ�Ϻ췯��(�ظ�����:Na2Cr2O7��2H2O)��Ҫ���Ը�����(��Ҫ�ɷ�ΪFeO��Cr2O3,������Al2O3��SiO2������)Ϊ��Ҫԭ������,����Ҫ������������:
���������Ҫ��Ӧ�Ļ�ѧ����ʽ����:
4FeO��Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
��1�� ���з�Ӧ���ڻ�תҤ�н��е�,��Ӧʱ�費�Ͻ���,���������� ��
��2�� ����Al2O3�ڢ���ת���Ļ�ѧ��Ӧ����ʽΪ������ ����
��3�� �û�ѧƽ���ƶ�ԭ��˵��������е���������������������������������������������������(�����ӷ���ʽ�������˵��),������pH���Ͳ�����Ӱ����������������������
��4�� �����ữ��ʹCrO42-ת��ΪCr2O72-д���÷�Ӧ�����ӷ���ʽ:�� ��
��5�� ��ҵ�ϻ����õ�ⷨ�Ʊ��ظ�����,��װ��ʾ��ͼ���ϡ�
�����ĵ缫��ӦʽΪ�� ;
�����ĵ缫��ӦʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں�PH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
��ʵ����ơ�����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K������ʵ���������±�����������¶Ա����顣
��1�����������ʵ����Ʊ������в�Ҫ���ո�
| ʵ�� ��� | ʵ��Ŀ�� | T/K | pH | c/10-3mol��L-1 | |
| H2O2 | Fe2+ | ||||
| �� | Ϊ����ʵ�����ο� | 298 | 3 | 6.0 | 0.30 |
| �� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | | | | |
| �� | | 298 | 10 | 6.0 | 0.30 |
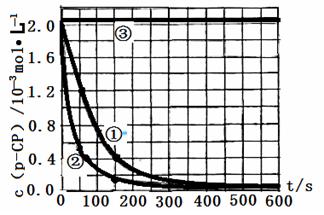
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й��������ε�ˮ���ص��ǣ� ��
| A��NH4Cl��ZnCl2��Һ�������ӽ���ʱ�ij���� |
| B����NaHCO3��Al2(SO4)3������Һ���Ƴ���ĭ���� |
| C�������²��NaHSO3��Һ��pHС��7 |
| D��ʵ����ʢ��Na2CO3��Һ���Լ�ƿ������ĥ�ڲ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com