
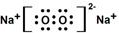 £¬øĆĪļÖŹĖłŗ¬ÓŠµÄĪ¢Į£¼ä×÷ÓĆĮ¦µÄĄąŠĶĪŖĄė×Ó¼ü”¢¹²¼Ū¼ü£®
£¬øĆĪļÖŹĖłŗ¬ÓŠµÄĪ¢Į£¼ä×÷ÓĆĮ¦µÄĄąŠĶĪŖĄė×Ó¼ü”¢¹²¼Ū¼ü£®·ÖĪö Q”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ£¬Q”¢W”¢ZŹĒ·Ē½šŹōŌŖĖŲ£¬W”¢Z×īĶā²ćµē×ÓŹżĻąĶ¬£¬ZµÄŗĖµēŗÉŹżŹĒWµÄ2±¶£¬ŌņWĪŖOŌŖĖŲ”¢ZĪŖSŌŖĖŲ£»X”¢YŹĒ½šŹōŌŖĖŲ£¬XŹĒĶ¬ÖÜĘŚÖŠ½šŹōŠŌ×īĒæµÄŌŖĖŲ£¬ŌņX“¦ÓŚIA×壬Ō×ÓŠņŹż“óÓŚŃõ£¬¹ŹXĪŖNa£»ĪåÖÖŌŖĖŲŌ×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ21£¬ŌņQ”¢YµÄ×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ21-1-12=8£¬ĪåÖÖŌŖĖŲŗĖµēŗÉŹżÖ®ŗĶĪŖ55£¬Q”¢YµÄŗĖµēŗÉŹżÖ®ŗĶĪŖ55-11-8-16=20£¬ĒŅYĪŖ½šŹō£¬æÉĶĘÖŖQĪŖNŌŖĖŲ”¢YĪŖAl£®
½ā“š ½ā£ŗQ”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ£¬Q”¢W”¢ZŹĒ·Ē½šŹōŌŖĖŲ£¬W”¢Z×īĶā²ćµē×ÓŹżĻąĶ¬£¬ZµÄŗĖµēŗÉŹżŹĒWµÄ2±¶£¬ŌņWĪŖOŌŖĖŲ”¢ZĪŖSŌŖĖŲ£»X”¢YŹĒ½šŹōŌŖĖŲ£¬XŹĒĶ¬ÖÜĘŚÖŠ½šŹōŠŌ×īĒæµÄŌŖĖŲ£¬ŌņX“¦ÓŚIA×壬Ō×ÓŠņŹż“óÓŚŃõ£¬¹ŹXĪŖNa£»ĪåÖÖŌŖĖŲŌ×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ21£¬ŌņQ”¢YµÄ×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ21-1-12=8£¬ĪåÖÖŌŖĖŲŗĖµēŗÉŹżÖ®ŗĶĪŖ55£¬Q”¢YµÄŗĖµēŗÉŹżÖ®ŗĶĪŖ55-11-8-16=20£¬ĒŅYĪŖ½šŹō£¬æÉĶĘÖŖQĪŖNŌŖĖŲ”¢YĪŖAl£®
£Ø1£©NŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÓŚµŚ¶žÖÜĘŚµŚVA ×壻¹Ź“š°øĪŖ£ŗµŚ¶žÖÜĘŚµŚVA ×壻
£Ø2£©X”¢Y×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·Ö±šĪŖNaOHÓėAl£ØOH£©3£¬¶žÕß·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗAl£ØOH£©3+OH-=AlO2-+2H2O£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3+OH-=AlO2-+2H2O£»
£Ø3£©NaŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉNa2O2£¬Ęäµē×ÓŹ½ŹĒ 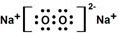 £»ŌŚøĆĪļÖŹŗ¬ÓŠµÄ»Æѧ¼üŹĒĄė×Ó¼ü”¢¹²¼Ū¼ü£¬
£»ŌŚøĆĪļÖŹŗ¬ÓŠµÄ»Æѧ¼üŹĒĄė×Ó¼ü”¢¹²¼Ū¼ü£¬
¹Ź“š°øĪŖ£ŗ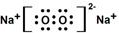 £»Ąė×Ó¼ü”¢¹²¼Ū¼ü£»
£»Ąė×Ó¼ü”¢¹²¼Ū¼ü£»
£Ø4£©H2SÓŠ»¹ŌŠŌ£¬¶ų H2O2ÓŠŃõ»ÆŠŌ£¬¶žÕß·¢ÉśŃõ»Æ»¹Ō·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗH2S+H2O2=S”ż+2H2O£¬
¹Ź“š°øĪŖ£ŗH2S+H2O2 =S”ż+2H2O£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶĘĄķÄÜĮ¦”¢ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬ÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
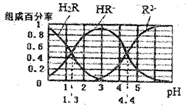
| A£® | ŌŚpH=4.4µÄČÜŅŗÖŠ£ŗ3c£ØHR-£©=c£ØNa+£©+c£ØH+£©-c£ØOH-£© | |
| B£® | µČĢå»żµČÅØ¶ČµÄNaOHČÜŅŗÓėH2RČÜŅŗ»ģŗĻŗó£¬ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č±Č“æĖ®Š” | |
| C£® | ŌŚpH=3µÄČÜŅŗÖŠ“ęŌŚ $\frac{c£Ø{R}^{2-}£©”Įc£Ø{H}_{2}R£©}{c£ØH{R}^{-}£©^{2}}$=10-3.1 | |
| D£® | ĻņNa2CO3ČÜŅŗÖŠ¼ÓČėÉŁĮæH2RČÜŅŗ£¬·¢Éś·“Ó¦£ŗCO32-+H2R=HCO3-+HR- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1mol/L NaHCO3ČÜŅŗÓė0.1mol/L NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ£ŗC£ØNa+£©£¾c£ØCO32-£©£¾c£ØHCO3- £©£¾c£ØOH-£© | |
| B£® | 20ml 0.1mol/L CH3COONaČÜŅŗÓė10ml0.1mol/L HClČÜŅŗ»ģŗĻŗóČÜŅŗ³ŹĖįŠŌ£¬ĖłµĆČÜÖŠ£ŗC£ØCH3COO-£©£¾c£ØCl-£©£¾c£ØCH3COOH£©£¾c£ØH+£© | |
| C£® | ŹŅĪĀĻĀ£¬pH=2µÄŃĪĖįÓėpH=12µÄ°±Ė®µČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ£ŗc£ØCl-£©+c£ØH+£©£¾c£ØNH4+ £©+c£ØOH-£© | |
| D£® | 0.1mol/L CH3COOHČÜŅŗÓė0.1mol/L NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ£ŗc£ØOH-£©£¾c£ØH+£©+c£ØCH3COOH£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĄūÓĆČēĶ¼×°ÖĆ²ā¶ØÖŠŗĶČȵďµŃé²½ÖčČēĻĀ£ŗ
ĄūÓĆČēĶ¼×°ÖĆ²ā¶ØÖŠŗĶČȵďµŃé²½ÖčČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2µÄµē×ÓŹ½ 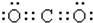 | |
| B£® | Cl-µÄ½į¹¹Ź¾ŅāĶ¼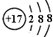 | |
| C£® | NaOHµÄµē×ÓŹ½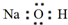 | |
| D£® | Ō×ÓŗĖÄŚÓŠ20øöÖŠ×ÓµÄĀČŌ×Ó${\;}_{17}^{37}$Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na”¢Al”¢Fe½šŹōµ„ÖŹŌŚŅ»¶ØĢõ¼žĻĀÓėĖ®·“Ó¦¶¼Éś³ÉH2ŗĶ¶ŌÓ¦µÄ¼ī | |
| B£® | H2O2”¢Na202”¢SO2¶¼¾ßÓŠĘư׊ŌĒŅĘÆ°×ŌĄķĻąĶ¬ | |
| C£® | ±„ŗĶNa2C03ČÜŅŗÖŠĶØČėCO2ČÜŅŗ»į±ä»ė×Ē | |
| D£® | æÉÓĆŹÆ»ŅĖ®ĪüŹÕĪ²ĘųÖŠµÄS02ĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ĖÄĀČ»ÆĢ¼
ĖÄĀČ»ÆĢ¼ CO2
CO2 HClO
HClO ĀČ»Æļ§
ĀČ»Æļ§ Na2O2
Na2O2

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com