
��17�֣���������ϡ�������ij��ʯ�����Һ�У����˺��д��������⣬����������NH4+��Fe3����AsO43����Cl����Ϊ��ȥ�������ӣ����ֲ����������£�
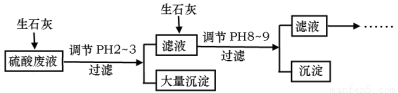
��ش����⣺
��1����ϡ�������ij��ʯ�����Һ�У������Ũ��Ϊ4.9g��L��1�������Һ�е�pHԼΪ ��
��2��NH4+����ϡ�������ij��ʯ�����Һ����(NH4)2SO4��NH4Cl��ʽ���ڡ�����һ��(NH4)2SO4��Һ��һ��NH4Cl��Һ��(NH4)2SO4��Һ��c(NH4��)ǡ����NH4Cl��Һ��c(NH4��)��2������c[(NH4)2SO4] c(NH4Cl)�������=����
��3���������Һ��Ͷ����ʯ�ң�������Һ�¶ȵı仯������Һ�� _______(���������С�����䡱)��
_______(���������С�����䡱)��
��4��Ͷ����ʯ�ҵ���pH��2~3ʱ������������Ҫ�ɷ�ΪCaSO4��2H2O[��������Fe(OH)3]���ᴿCaSO4��2H2O����Ҫ�������裺������м������ ����ַ�Ӧ���ˡ�ϴ�ӡ� ��
��5��25��, H3AsO4���볣��ΪK1=5.6��10��3��K2=1.7��10��7��K3=4.0��10��12������Һ��pH���ڵ�8~9ʱ��������Ҫ�ɷ�ΪCa3(AsO4)2��
��pH���ڵ�8����Ca3(AsO4)2�ſ�ʼ������ԭ���� ��
��Na3AsO4��һ��ˮ���ƽ�ⳣ����ֵΪ�� ��
����֪��AsO43��+2I��+2H+= AsO33��+I2+H2O ��SO2+I2+2H2O=SO42��+2I��+4H+ ������������Ӧ�л�ԭ����ǿ������ ��
��1��1��2���� ��3����С��4��ϡ���� ���ɻ���� ��5����H3AsO4�����ᣬ����Һ��pH���ڵ�8���ң�c(AsO43��)����Ca3(AsO4)2��ʼ���� ��2.5��10��3 ��SO2 ��
��������
�����������1����������Ũ��Ϊ4.9g��L��1���������ʵ���Ũ��Ϊ0.05mol/L���Ӷ�c(H��)=0.1mol/L,ȷ��pH=1����2�����ӵ�Ũ��ԽС��ˮ��̶�Խ������(NH4)2SO4��Һ��c(NH4��)ǡ����NH4Cl��Һ��c(NH4��)��2��������c[(NH4)2SO4 ] < c(NH4Cl);(3)Ͷ����ʯ�ң���Һ��c(OH��)������Һ�к���������NH4��,���Ա�ֵ��С����4���ᴿCaSO4��2H2O����Ϊ����������Fe(OH)3��Ӧ������м��������ϡ���ᣬ��ϴ�Ӻ��ڸ����5����ΪH3AsO4�����ᣬ����Һ��pH���ڵ�8���ң�c(AsO43��)����Ca3(AsO4)2��ʼ��������ˮ�ⷽ��ʽ��AsO43����H2O=HAsO42����OH����ˮ��ƽ�ⳣ��Kh=c(HAsO42��)c(OH��)/c(AsO43��),K3=c(AsO42��)c(H+)/c(HAsO42��),KW=c(H+)c(OH��),����KW=Kh��K3���Ӷ����ˮ��ƽ�ⳣ��Ϊ
2.5��10��3 �����е�����������ԭ��Ӧ�У���ԭ�ԣ�SO2>I��>AsO33��.
���㣺��Ϲ������̵�����ˮ�⡢���ӡ���������ԭ��Ӧ��
��������� ����1�����ʵķ��롢���Ӻ��ᴿ ����2�����ʵļ���ͼ��� ��������

 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡտ���и����߿����ԣ�һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣���ҵ����������ˮ��̼���ȣ�SrCO3����ĩΪԭ��(�������������Ļ�����)�Ʊ��ߴ���ˮ�Ȼ��Ⱦ���(SrCl2��6H2O)�������Ϊ��

��֪����.�й��������������pH��
�������� | Fe(OH)3 | Fe(OH)2 |
��ʼ������pH | 1.5 | 6.5 |
������ȫ��pH | 3.7 | 9.7 |
��.SrCl2��6H2O ������61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ��
��1����������Ҫ�ӿ췴Ӧ���ʣ���ʩ�г�ֽ���� ��дһ�֣���
̼���������ᷴӦ�����ӷ���ʽ ��
��2���ڲ����-�۵Ĺ����У�����Һ��pHֵ��1������ �����õ��Լ�Ϊ ��
A��1.5
B��3.7
C��9.7
D����ˮ
E���������ȷ�ĩ
F��̼���ƾ���
��3����������������������Ҫ�ɷ��� (�ѧʽ)��
��4����ҵ�����ȷ紵����ˮ�Ȼ��ȣ����˵��¶���
A��50~60�� B��80~100�� C��100������
��5���������ѡ�õ���ϴ�Ӽ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и���������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����Cl-��I-��ϡ��Һ�е���AgNO3��Һ�����������������AgNO3��Һ����Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
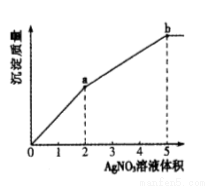
A��KSP (AgCl) < KSP (AgI)
B��c( Cl- ) ��c( I-) = 3 ��2
C��m( AgCl ) ��m( AgI ) = 2 ��3
D��a��b�β�����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����б����ܶ�Ա������ѧģ�����������3�������棩 ���ͣ������
��16�֣�NO��NO2�dz����ĵ�������о����ǵ��ۺ���������Ҫ���塣
��1��������������Ļ��������� ����һ�֣���
��2����������ԭ���������������ת�����£�
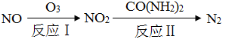
�ٷ�Ӧ��Ϊ��NO��O3��NO2��O2������11.2 L O2����״����ʱ��ת�Ƶ��ӵ����ʵ����� mol��
�ڷ�Ӧ���У���n(NO2)��n[CO(NH2)2]��3��2ʱ����Ӧ�Ļ�ѧ����ʽ�� ��
��3����������һ�ֹ��ϵ���������ķ�����ͬʱʵ���˵��������ѭ��ת������Ҫ��ӦΪ��
NO2(g)��SO2(g) SO3(g)��NO(g) ��H����41.8 kJ��mol��1
SO3(g)��NO(g) ��H����41.8 kJ��mol��1
����֪��2SO2(g)��O2(g) 2SO3(g) ��H����196.6 kJ��mol��1
2SO3(g) ��H����196.6 kJ��mol��1
д��NO��O2��Ӧ����NO2���Ȼ�ѧ����ʽ ��
��һ���¶��£���2 L�����ܱ������г���NO2��SO2��1 mol��5min�ﵽƽ�⣬��ʱ������NO ��NO2��Ũ��֮��Ϊ3��1����NO2��ƽ��ת������ ��
��������Ӧ��ƽ���������������ʱ������������ͬʱ����
NO2��SO2��SO3��NO��1mol��ƽ�� ������ţ���
A��������Ӧ�����ƶ�
B�����淴Ӧ�����ƶ�
C�����ƶ�
��4��ij��ѧ��ȤС�鹹�뽫NOת��ΪHNO3��װ����ͼ���缫Ϊ����Բ��ϡ����ĵ缫��Ӧʽ�� ��
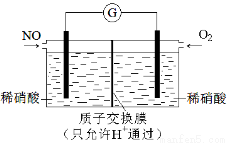
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����б����ܶ�Ա������ѧģ�����������3�������棩 ���ͣ�ѡ����
���ıࡿ�����л���Ľṹ�������йص�������ȷ����
A����ϩͨ������KMn04��Һ�У���ɫ��ȥ������Ϊ�����˼ӳɷ�Ӧ
B�����ࡢ��֬�������ʶ�������Ȼ�߷��ӻ�����
C�������ǣ����ǵķ���ʽ��ΪC6H12O6������Ϊͬ���칹��
D�������ȵ�NaOH��Һ��ȥ���������е���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�ൺ�и�����ѧ��һģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��10.7gMg��Al��Fe��ɵĺϽ���������������������Һ�У�������״����3.36L���塣��ȡ�������ĺϽ����ڹ��������У����ɱ�״����7.84L���壬��Ӧ�����Һ�м������NaOH��Һ���õ��������ʵ���Ϊ
A��0.1mol B��0.2mol C��0.25mol D��0.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��У������һ��ʮУ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��15�֣���������ƣ�Na2S2O3��5H2O�����������մ��ֳ�Ϊ��������������������ҵ����Ӱ����Ҳ������ֽ��Ư�������ȼ��ȡ���������ˮ���������Ҵ������ȡ�������ֽ⡣��ҵ�ϳ����������Ʒ�������Ʊ���ijʵ����ģ�ҵ���ȡ��������ƣ��䷴Ӧװ�ü������Լ�����ͼ��
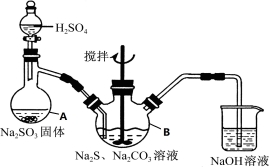
ʵ������������Ϊ��
�ٿ�����Һ©����ʹ�����������£��ʵ����ڷ�Һ�ĵ��٣�ʹ��Ӧ������SO2����Ͼ��ȵ�ͨ��Na2S��Na2CO3�Ļ����Һ�У�ͬʱ�����綯������������ˮԡ���ȣ��С�
��ֱ�������Ļ��Dz�����ʧ����������Һ��pH�ӽ�7ʱ��ֹͣͨ��SO2���塣
�۳��ȹ��ˣ�����Һ����Ũ������ȴ����Na2S2O3��5H2O��
���پ����ˡ�ϴ�ӡ�����õ�����IJ�Ʒ��
��1��д������A������ �������ϴ��ʱ��Ϊ�˼��ٲ������ʧ�õ��Լ������� ��
��2��Ϊ�˱�֤��������ƵIJ�����ʵ���в�������ҺpH<7���������ӷ���ʽ����ԭ�� ��
��3��д��������ƿB����ȡNa2S2O3��Ӧ���ܻ�ѧ��Ӧ����ʽ ��
��4�����õ��IJ�Ʒ�п��ܺ���Na2SO4���ʡ������ʵ�����Ʒ���Ƿ����Na2SO4����Ҫ˵��ʵ�����������ͽ��ۣ� ��
��5���ⶨ��Ʒ����
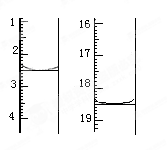
ȷ��ȡ1.00 g��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0��100 0 mol��L��1��ı���Һ�ζ�����Ӧԭ��Ϊ2S2O32-��I2===S4O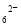 ��2I�����ζ���ʼ���յ��Һ��λ����ͼ�������ĵ�ı���Һ���Ϊ_______mL����Ʒ�Ĵ���Ϊ %��
��2I�����ζ���ʼ���յ��Һ��λ����ͼ�������ĵ�ı���Һ���Ϊ_______mL����Ʒ�Ĵ���Ϊ %��
��6��Na2S2O3���������ȼ�������Һ���ױ�Cl2������SO42�����÷�Ӧ�����ӷ���ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��ɫ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�绯ѧ����NO3-��ԭ����ͼ��ʾ������˵������ȷ����

A��Ǧ���ص�A��Ϊ�������缫����ΪPb
B��Ǧ���ع���������ÿͨ����·��2mol����������1molH2SO4
C���õ��ص�������ӦΪ2NO3- + 12H�� + 10e- �� N2�� + 6H2O
D������������ת��5moL���ӣ���Ĥ������Һ�������仯���m��m�ң�Ϊ14��4g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и���һģ��ѧ�Ծ��������棩 ���ͣ������
��17�֣�ͭ�ڹ�ũҵ���������Ź㷺����;��
��1������CuSO4��Һʱ���������ϡH2SO4����ԭ���� ��ֻд���ӷ���ʽ����
��2��ijͬѧ�����Ƶõ�CuSO4��Һ����������ʵ��̽����
��ͼ���Ǹ��ݷ�ӦFe+CuSO4=Cu+FeSO4��Ƴ���ͭԭ��أ���ͼ���еĺ�������ɱ�ע��
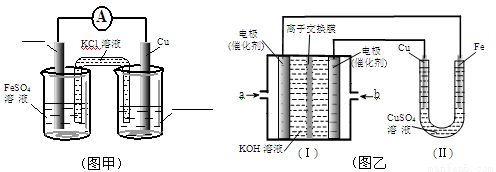
��ͼ���У�I�Ǽ���ȼ�ϵ�ص�ʾ��ͼ����ͬѧ����II��ʵ�����϶�ͭ����Ӧ��a��ͨ�� (�CH4����O2��)��b���缫�Ϸ����ĵ缫��ӦʽΪ ==4OH-��
����II�е缫����Ϊ���Ե缫�����Һ��Ϊ����0.1molNaCl��Һ400mL������������������Ϊ448mL(��״����)ʱ����Һ��pH= ��������Һ����仯���Բ���)��
��3�����������ҵ��ˮ�г����ж���Cu2+���ؽ������ӣ�����FeS������������Ϊ��������ȥ[������Ksp(FeS)��6.3��10��18mol2��L��2��Ksp(CuS)��1.3��10��36mol2��L��2]���������ӷ���ʽ˵���������ӵ�ԭ��������FeS���빤ҵ��ˮ�к�ֱ��FeSȫ��ת��ΪCuS�������Ӷ���ȥ��Һ��Cu2+��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com