
��20 mL HCl��H2SO4�Ļ����Һ����μ���0.1 mol��L-1��Ba(OH)2��Һ�����ɳ�������������Һ��pH������Ba(OH)2��Һ����Ĺ�ϵ��ͼ5��ʾ��������������⣺
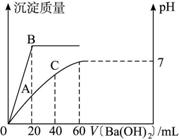
ͼ5
(1)��ʼʱ�����������������ʵ���Ũ��Ϊ______________ mol��L-1��
(2)��ʼʱ�����������������ʵ���Ũ��Ϊ______________ mol��L-1��
(3)B���ʾ�ij���������Ϊ______________g��
(4)A���ʾ��Һ�еģ�H+��Ϊ______________ mol��L-1��pHΪ______________��
(5)C���pHΪ______________(pH��ֱ���ö�����ʾ)��
(1)0.1
(2)0.4
(3)0.466
(4)0.2 07
(5)1.18��-lg![]()
Ba2++![]() ====BaSO4��
====BaSO4��
H+ + OH-====H2O
1 1 1
n(![]() )=n��Ba(OH)2��=0.02 L��0.1 mol��L-1=2��10-3 mol
)=n��Ba(OH)2��=0.02 L��0.1 mol��L-1=2��10-3 mol
c(H2SO4)=n(H2SO4)/V(aq)=2��10-3 mol/002 L=0.1 mol��L-1
n(H+)=2��0.06 L��0.1 mol��L-1=0.012 mol
n(HCl)=n(H+)-2n(H2SO4)=0.012 mol-2��0.002 mol=0.008 mol
c(HCl)=n(HCl)/V(aq)=0.008 mol/0.02 L=0.4 mol��L-1
n(BaSO4)=n(![]() )=0.002 mol
)=0.002 mol
m(BaSO4)=n(BaSO4)��M(BaSO4)=0.002 mol��233 g��mol-1=0.466 g
(4)��A��ʱ��Ba(OH)2ǡ����H2SO4��ȫ��Ӧ����ʱ��Һ��ʣ���H+ȫ����HCl�ģ�n(H+)=n(HCl)=0.008 mol�����ԣ�c(H+)=n(H+)/V(��)=0.008 mol/0.04 L=0.2 mol��L-1,pH=-lg 0.2=0.7��
(5)C��ʱ�Ļ��Һ����A��Ļ������ֵ���20 mL Ba(OH)2��Һ����ʱBa(OH)2ֻ��HCl��Ӧ��ʣ���H+��n(H+)=0.008 mol-2n��Ba(OH)2��=0.008 mol-2��0.1 mol��L-1��0.02 L=0.004 mol,c(H+)=0.004 mol/0.06 L=1/15 mol��L-1��pH=-lg![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

ͼ5
(1)��ʼʱ�����������������ʵ���Ũ��Ϊ______________ mol��L-1��
(2)��ʼʱ�����������������ʵ���Ũ��Ϊ______________ mol��L-1��
(3)B���ʾ�ij���������Ϊ______________g��
(4)A���ʾ��Һ�еģ�H+��Ϊ______________ mol��L-1��pHΪ______________��
(5)C���pHΪ______________(pH��ֱ���ö�����ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ѧ��ѧ��Ӧԭ��������������⣺
��1��ij��Һ��������ͬ���ʵ��������ʣ�������ֻ����OHһ��H����![]() ��Clһ�������ӣ���c��
��Clһ�������ӣ���c��![]() ��>c��Cl����>c��OH����>c��H��������������������_____________��
��>c��Cl����>c��OH����>c��H��������������������_____________��
��2��0��1 mol��L��1�İ�ˮ��0��05 mol��L��1��ϡ����������ϣ������ӷ���ʽ��ʾ��Ϻ���Һ������ԣ�______________________��
��3����֪��Ksp��RX����1��8��10��10��Ksp��RY����1��5��10��16��Ksp��R2Z����2��0��10��12����������RX��RY��R2Z�ı�����Һ�У�R��Ũ���ɴ�С��˳����_____________��
��4����ʯī�缫���100 mL 0��1 mol��L��1CuSO4��Һ���������ϲ�����������ʵ���Ϊ0��01 mol��������������Cu������Ϊ__________g��
��5����20 mL���������Ļ��Һ����μ���pH��13��Ba��OH��2��Һ������BaSO4��������ͼ��ʾ��B����Һ��pH��7�������������ֱ����ӣ�����c��HCl����_______mol��L��1.

��6�����¶ȡ��ݻ���ͬ��3���ܱ������У����±�Ͷ�뷴Ӧ�������Ӧ��H2��g����I2��g��![]() 2HI��g�� ��H����14��9 kJ��mol��1�����ں��¡����������£���÷�Ӧ�ﵽƽ��ʱ���������±���
2HI��g�� ��H����14��9 kJ��mol��1�����ں��¡����������£���÷�Ӧ�ﵽƽ��ʱ���������±���

����˵����ȷ����_______________��
A��![]() ��
��![]() ��1 B��2
��1 B��2![]() ��
��![]() C��a��b��14��9 D��c1��c2��c3
C��a��b��14��9 D��c1��c2��c3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ֣���и߶���ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣� ������ѧ��ѧ��Ӧԭ��������������⣺
��1��ij��Һ��������ͬ���ʵ��������ʣ���Һ��ֻ����OH����H����NH4����Cl���������ӣ���c��NH4������c��Cl������c��OH������c��H�������������������� _________ ��
��2��0.1 mol��L-1�İ�ˮ��0.05 mol��L-1��ϡ����������ϣ������ӷ���ʽ��ʾ��Ϻ���Һ������ԣ� ��
��3����ʯī�缫���100 mL 0.1 mol��L-1CuSO4��Һ���������ϲ�����������ʵ���Ϊ0.01 mol��������������Cu������Ϊ g��
��4����AgCl�ֱ�����5mL H2O ��10mL0.2mol��L-1 MgCl2 ��20 mL0.5mol��L-1 NaCl��Һ ��40 mL0.1mol��L-1HCl���ܽ������ͣ�����Һ��Ag+��Ũ���ɴ�С��˳����________________��
��5����20 mL���������Ļ��Һ����μ���pH��13��Ba(OH)2��Һ������BaSO4��������ͼ��ʾ��B����Һ��pH��7��������Һ����仯������c��HCl����_________mol��L-1��
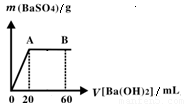
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���㽭ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
(12�֣�������ѧ��ѧ��Ӧԭ��������������⣺
��1��ij��Һ��������ͬ���ʵ��������ʣ�������ֻ����OHһ��H����NH4+��Clһ�������ӣ�
��c(NH4+)>c(Cl��)>c(OH��)>c(H��)���������������� ��
��2��0.1 mol��L��1�İ�ˮ��0.05 mol��L��1��ϡ����������ϣ������ӷ���ʽ��ʾ��Ϻ���Һ������ԣ� ��
��3����֪��Ksp(RX)��1��8��10��10��Ksp(RY)��1��5��10��16��Ksp(R2Z)��2��0��10��12����������RX��RY��R2Z�ı�����Һ�У�R��Ũ���ɴ�С��˳���� ��
��4����20 mL���������Ļ��Һ����μ���pH��13��Ba(OH)2��Һ������BaSO4����
����ͼ��ʾ��B����Һ��pH��7(�������
����ֱ�����)����c(HCl)�� mol��L��1.

��5�����¶ȡ��ݻ���ͬ��3���ܱ������У�
���±�Ͷ�뷴Ӧ�������Ӧ(H2(g)��
I2(g) 2HI(g) ��H����14.9 kJ��mol��1)���ں��¡�����������, ��÷�Ӧ��
2HI(g) ��H����14.9 kJ��mol��1)���ں��¡�����������, ��÷�Ӧ��
��ƽ��ʱ���������±���
����˵����ȷ���� ��
A�� ��
�� ��1
B��2
��1
B��2 ��
�� C��a��b��14.9
D��c1��c2��c3
C��a��b��14.9
D��c1��c2��c3

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com