
雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH 、Mg2+、Al3+、SO
、Mg2+、Al3+、SO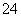 、NO
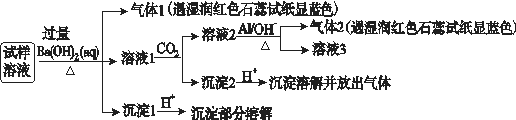
、NO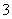 、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验:
、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验:
已知:3NO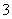 +8Al+5OH-+2H2O=3NH3↑+8AlO
+8Al+5OH-+2H2O=3NH3↑+8AlO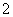
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A.试样中肯定存在NH 、Mg2+、SO
、Mg2+、SO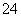 和NO
和NO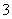 B.试样中可能存在Na+、Cl-
B.试样中可能存在Na+、Cl-
C.该雾霾中可能存在NaNO3、NH4Cl和MgSO4 D.试样中一定不含Al3+
【知识点】离子推断 B1 B2
【答案解析】D 解析:试样溶液中加入过量Ba(OH)2并加热,生成的气体1能使湿润的红色石蕊试纸变蓝色,说明气体1是NH3,则试样中含有NH4+;
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐,也有可能是试样中存在Al3+,在过量的Ba(OH)2中反应生成AlO2-,通入CO2后生成Al(OH)3沉淀;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,以及能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+
A、通过以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,故A正确;
B、通过以上分析知,试样中可能存在Na+、Cl-,故B正确;
C、根据以上分析知,试样中肯定存在NH4+、Mg2+、SO42-和NO3-,可能存在Na+、Cl-,所以该雾霾中可能存在NaNO3、NH4Cl和MgSO4,故C正确;
D、通过以上分析知,试样中不能确定是否含有Al3+,故D错误;
【思路点拨】本题考查了物质的推断,明确物质的性质及特殊反应现象是解本题关键,根据物质的溶解性、物质的性质及题给信息来分析解答,题目难度中等.


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好。某种金丝桃素的结构简式如图所示:
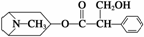
下列有关金丝桃素的说法:
①属于烃的衍生物,燃烧只产生CO2和H2O ②可以发生取代、加成、酯化、消去等反应 ③分子式为C17H23NO3,苯环上的一氯取代物有3种 ④1 mol该物质最多能和6 mol H2发生加成反应
其中错误的是( )
A.①和④ B.②和③ C.①和③ D.②和④
查看答案和解析>>
科目:高中化学 来源: 题型:
能够证明甲烷构型是正四面体的事实是( )
A.甲烷的四个键键能相同
B.甲烷的四个键键长相等
C.甲烷的所有C—H键键角相等
D.二氯甲烷没有同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化工生产的说法中,不正确的是( )
A.工业上用热还原法冶炼铁:Fe2O3+3CO 3CO2+2Fe
3CO2+2Fe
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.在铁管上镀锌,用铁管作阳极,锌块作阴极
D.利用反应:NaCl(饱和)+CO2+NH3+H2O====NaHCO3↓+NH4Cl制取NaHCO3时,应先通入过量的NH3,再通入过量的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
银铜合金广泛用于航空工业,从切割废料中回收银并制备铜化工产品的工艺如下:
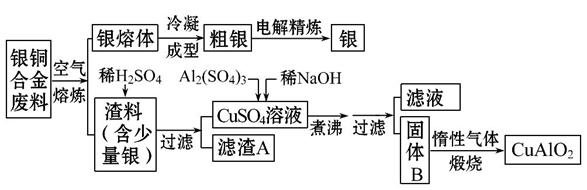
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为__________;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为____________
____________________________________________________。
(2)固体混合物B的组成为____________;在生成固体B的过程中,需控制NaOH的加入量。若NaOH过量,则因过量引起的反应的离子方程式为______________
____________________________________________________。
(3)完成煅烧过程中一个反应的化学方程式:
______CuO+____Al2O3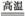 ______CuAlO2+____↑。
______CuAlO2+____↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0 kg废料中的铜可完全转化为________mol CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液____________L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是__________、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中一定能大量共存的是
①透明溶液中:K+、Fe3+、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、Br-、SO42-、NH4+
④由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ca2+、Cl-、Br-
⑤有较多Fe3+的溶液中: Na+、NH4+、Cl-、HCO3-
⑥酸性溶液中:Fe2+、Al3+、NO3-、Cl-
A.①② B.③⑥ C.②④ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%)。某同学设计了如下方案,分离样品中各种金属元素。请回答下列问题。
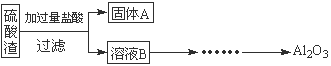
(1)写出溶液B的溶质是 。
(2)参照以下框图形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作) 。
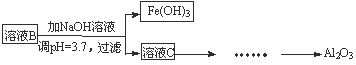
(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。写出反应的离方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,含有CCl4, I2, I-等)中回收碘,其实验过程如下:
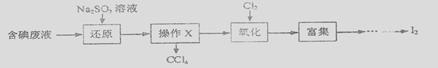
(1)操作x的名称为________________。主要的仪器是_______________________。
(2)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的 I2 还原为I-,其离子方程式为_________;该操作的目的是____________________。
(3)①在测定亚硫酸钠溶液浓度时,量取25.00mL亚硫酸钠溶液,用0.10mol·L-1的酸性高锰酸钾溶液进行滴定,下列说法正确的是_________________。
A.润洗滴定管时,应从滴定管上口加满所需的试液,使滴定管内壁充分润洗
B.高锰酸钾溶液装在酸式滴定管中,本实验无需外加指示剂
C.滴定时,眼睛注视滴定管中液面的变化
D.滴定开始时读数正确,滴定终点仰视读数,会使实验误差偏高
②达到滴定终点时,消耗高锰酸钾溶液18.00mL,则亚硫酸钠溶液的浓度为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )
A.丙烷与氯气在光照条件下生成氯丙烷
B.乙烯与溴的四氯化碳溶液反应生成1,2二溴乙烷
C.乙烯与水反应生成乙醇
D.乙烯自身聚合生成聚乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com