
【题目】化学与生活、生产密切相关。下列叙述正确的是
A. 酯在碱性条件下的水解反应叫皂化反应![]()
B. 橡胶、合成塑料、合成纤维均是人工合成的高分子材料
C. 古代四大发明中“黑火药”的成分是“一硫二硝三木炭”,这里的“硝”指的足硝酸
D. 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,反应 3A(g)+3B(g) c(g)+D(g) ΔH<0 达到平衡,欲提高B的转化率,可采取的措施是( )
A.升高温度B.增大 B 的浓度C.增大压强D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的下列叙述中,正确的是( )
A.离子化合物可能含共价键
B.共价化合物可能含离子键
C.离子化合物中只含离子键
D.共价化合物中可能含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯与乙烷的混合气体共 amol,与 bmol 氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2 的混合气体和 45g 水,则下列说法错误的是( )
A. 当 a=1 时,乙烯和乙烷的物质的量之比为 1:1
B. 当 a=1 时,且反应后CO和CO2 的混合气体的物质的量为反应前氧气的![]() 时,则b=3
时,则b=3
C. 当 a=1 时,且反应后 CO 和 CO2 的混合气体的物质的量为反应前氧气的![]() 时,则 CO 和 CO2 的物质的量之比为 3:1
时,则 CO 和 CO2 的物质的量之比为 3:1
D. a 的取值范围为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对大气污染物NOx进行研究具有重要环保意义。
(1)已知汽车汽缸中生成NO的反应为:N2(g)+O2(g)![]() 2NO(g)-Q。若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在10.0 L密闭汽缸内经过5s反应达到平衡,测得NO为0.02mol/L。请回答下列问题:5s内该反应的平均速率ν(N2)=_____________。 汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是:______________________________。
2NO(g)-Q。若1.0 mol空气含0.80 mol N2和0.20 mol O2,1300oC时在10.0 L密闭汽缸内经过5s反应达到平衡,测得NO为0.02mol/L。请回答下列问题:5s内该反应的平均速率ν(N2)=_____________。 汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是:______________________________。
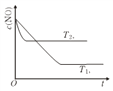
(2)右图表示在其他条件不变时,反应2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) 中,NO的浓度c(NO)在不同温度(T)下随时间(t)的变化曲线。该平衡的正向反应为_________反应 (填“吸热”或“放热”)。
2CO2(g)+N2(g) 中,NO的浓度c(NO)在不同温度(T)下随时间(t)的变化曲线。该平衡的正向反应为_________反应 (填“吸热”或“放热”)。
(3)为了减少汽车尾气对环境的污染,可采取的措施________________________(任写一个)。
另一方面,氮的许多化合物为我们人类生活带来便利。
(4)氨水是一种很好的氮肥,常温下测定0.1mol/L氨水溶液,其pH值小于13,其原因是_____(用电离方程式解释);常见氮肥种类有______________(列举两个)。
(5)硝酸铵易溶于水,其水溶液呈 ________(填“酸性”、“碱性”、或“中性”),原因是____________ (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在容积不变的密闭容器中注满NO2气体,2NO2(g)N2O4(g)△H<0.平衡后把该容器置于沸水中,下列性质或数值不会改变的是( )
①颜色 ②平均摩尔质量 ③质量 ④压强 ⑤密度.
A.①②
B.②③
C.④⑤
D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应达到平衡状态时,下列说法不正确的是( )
A. 正反应和逆反应同时进行,两者速率相等
B. 反应混合物的组成比例不会因时间而改变
C. 反应物和生成物同时存在,其浓度不再改变
D. 反应物和生成物的物质的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题进行计算:
(1)实验测得16g甲醇[CH3OH(l)]在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇燃烧热的热化学方程式: .
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)2NH3(g)△H=a kJmol﹣1 . 有关键能数据如表:
化学键 | H﹣H | N﹣H | N≡N |
键能(kJmol﹣1) | 436 | 391 | 945 |
试根据表中所列键能数据估算a的数值 .
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g)△H1=﹣393.5kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H2=﹣571.6kJmol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=﹣2599kJmol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:△H= .
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3﹣ . 两步反应的能量变化示
意图如图:
第一步反应是反应(填“放热”或“吸热”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是常用来衡量一个国家石油化工发展水平的标志性物质,A、B、C、D、E、F、G均为有机物,他们之间有如图转化关系,请回答下列问题:

(1)写出A中官能团的名称:A________ , B中官能团的电子式B________ 。
(2)在F的同系物中最简单的有机物的空间构型为________ 。
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的物质的结构简式:___________________________________________ 。
(4)写出下列编号对应反应的化学方程式,并注明反应类型:
④_____________________________ ,________反应 ;
⑦_____________________________ ,________反应 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com