
【题目】下列离子方程式书写正确且能合理解释事实的是( )
A.将铜丝插入稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
B.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时问后,溶液变蓝:4H++4I-+O2=2I2+2H2O
C.向Mg(HCO3)2溶液中加入过量NaOH溶液,产生白色沉淀:Mg2++2HCO![]() +2OH-=MgCO3↓+2H2O
+2OH-=MgCO3↓+2H2O
D.向含0.1molFeBr2的溶液中通入0.1molCl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
【答案】B
【解析】
A.将铜丝插入稀硝酸中,生成NO气体,3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故A错误;
B.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时问后,碘离子被空气中的氧气氧化生成碘单质,溶液变蓝:4H++4I-+O2=2I2+2H2O,故B正确;
C.Mg(OH)2比MgCO3更难电离,向Mg(HCO3)2溶液中加入过量NaOH溶液,产生氢氧化镁白色沉淀:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O,故C错误;
D.还原性:Fe2+>Br->Cl-,向含0.1molFeBr2的溶液中通入0.1molCl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】臭氧是一种强氧化剂可与碘化钾水溶液发生反应生成氧气和单质碘。向反应后的溶液中滴入酚酞,溶液变为红色。
(1)试写出该反应的化学方程式(Ⅰ):_____。
(2)该反应体系中还伴随着化学反应(Ⅱ):I2(aq) + I-(aq)![]() I3-(aq)。反应Ⅱ的平衡常数表达式为:____。
I3-(aq)。反应Ⅱ的平衡常数表达式为:____。
(3)根据如图,计算反应Ⅱ中3-18s内用I2表示的反应速率为_____。

(4)为探究Fe2+对上述O3氧化I-反应的影响,将O3通入含Fe2+和I-的混合溶液中。试预测因Fe2+的存在可能引发的化学反应(请用文字描述,如:“碘离子被臭氧氧化为碘单质”)① ______。② _____;该反应的过程能显著降低溶液的pH,并提高反应(Ⅰ)中Ⅰ-的转化率,原因是:____ 。
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢铁中的硫转化为H2SO3,然后以淀粉为指示剂,用一定浓度的I2溶液进行滴定。综合上述各步反应及已有知识,可推知氧化性强弱关系正确的是____(填序号)。
a. Fe3+> I2 b. O3> Fe3+ c. I2> O2 d. I2>SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙是一种白色固体,难溶于水,常用作杀菌剂、防腐剂。
(1)化学实验小组选用如图装置(部分固定装置略)用钙和氧气制备过氧化钙。
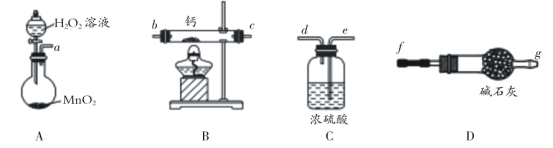
① 请选择装置,按气流方向连接顺序为 ___________(填仪器接口的字母编号)
② 实验室用A装置还可以制备 ______________ 等气体(至少两种)
③ 实验开始是先通氧气还是先点燃酒精灯?_________,原因是 ___________
(2)已知化学反应 Ca2+ + H2O2 + 2NH3 + 8H2O=CaO28H2O↓+ 2NH4+。在碱性环境中制取 CaO28H2O 的装置如图所示:
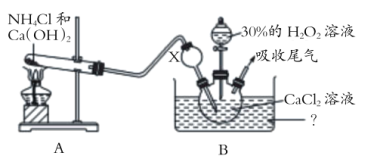
①写出 A 装置中发生反应的化学方程式:____________。
②为防止双氧水的分解并有利于 _________,装置 B 中应采用 ___________ 条件,装置 X 的作用是 ______________。
③ 反应结束后,经 _________、__________、低温烘干获得CaO28H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4与Cl2生成CH3Cl的反应过程中,中间态物质的能量关系如下图所示(Ea表示活化能),下列说法不正确的是
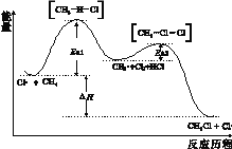
A. 已知Cl·是由Cl2在光照条件下化学键断裂生成的,该过程可表示为:![]()
B. 相同条件下,Ea越大反应速率越慢
C. 图中ΔH<0,其大小与Ea1、Ea2无关
D. CH4转化为CH3Cl的过程中,所有C-H发生了断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3mol A和2.5mol B混合于2L恒容的密闭容器中,保持温度不变发生的反应如下:3A(g)+B(g)![]() xC(g)+2D(g),反应5min达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min),下列结论正确的是( )
xC(g)+2D(g),反应5min达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min),下列结论正确的是( )
A.A的平均反应速率为0.10mol/(L·s)
B.平衡时,B的转化率为20%
C.平衡时,C的浓度为0.125mol/L
D.平衡时,容器内压强为原来的0.8倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态或气态碘分别与氢气反应的热化学方程式如下:
①H2(g)+I2(?)![]() 2HI(g) ΔH1=-9.48 kJ·mol-1
2HI(g) ΔH1=-9.48 kJ·mol-1
②H2(g)+I2(?)![]() 2HI(g) ΔH2=+26.48 kJ·mol-1
2HI(g) ΔH2=+26.48 kJ·mol-1
下列判断不正确的是( )
A.①中的I2为气态,②中的I2为固态
B.②的反应物总能量比①的反应物总能量低
C.反应①的产物比反应②的产物热稳定性更好
D.1 mol固态碘升华时将吸热35.96 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员采用新型锰催化体系,选择性实现了简单酮与亚胺的芳环惰性C-H的活化反应。利用该反应制备化合物J的合成路线如下:

已知: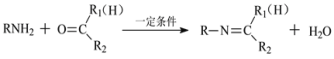
回答下列问题:
(1)A中官能团的名称是______。F的化学名称是______。
(2)C和D生成E的化学方程式为_____________。
(3)G的结构简式为________。
(4)由D生成F,E和H生成J的反应类型分别是______、_____。
(5)芳香化合物K是E的同分异构体。若K能发生银镜反应,则K可能的结构有____种,其中核磁共振氢谱有四组峰的结构简式为______(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上用ClO2气体制NaClO2的工艺流程如图所示。

下列说法不正确的是
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO2的离子方程式为2ClO2+H2O2=2ClO2-+2H+ +O2↑
C.工业上将ClO2气体制成NaCIO2固体,其主要目的是便于贮存和运输
D.通入的空气的目的是驱赶出ClO2,使其被吸收其充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将甲针筒内20mLH2S推入含有10 mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
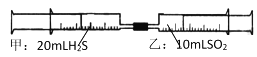
A. 有淡黄色固体生成
B. 有无色液体生成
C. 气体体积缩小
D. 最终约余15mL气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com