
| |||||||||||||||||||||||||||||||||
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:阅读理解
本题有I和II两小题。
Ⅰ.下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)其中标示出仪器使用温度的是__________(填写编号)。
(2)能够用以精确量取液体体积的是_______(填写编号)。
(3)由于操作错误,使得到的数据比正确数据偏小的是________(填写编号)。
A.用量筒量取一定量液体时,俯视液面读数
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容所得溶液的浓度
(4)称取10.5 g固体样品(1 g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为_________g。
(5)有下列实验:
①苯与溴的取代反应 ②苯的硝化反应
③乙醛的银镜反应 ④测定一定温度下KNO3的溶解度
⑤乙酸乙酯的制取 ⑥石油分馏实验
其中需要使用温度计的有___________(填写编号)
Ⅱ.某种胃药片的制酸剂为碳酸钙,其中所含的CaCO3质量的测定如下:
①需配制0.1 mol/L的HCl和0.1 mol/L的NaOH溶液;
②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后加入20.00 mL蒸馏水;
③以酚酞为指示剂,用0.1 mol/L的NaOH溶液滴定,需用去V mL达滴定终点;
④加入25.00 mL 0.1 mol/L的HCl溶液。
(1)写出实验步骤(写编号顺序)___________________________。
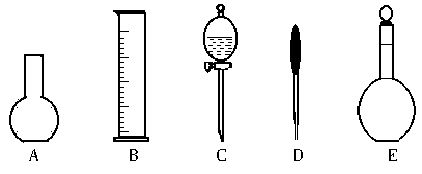
(2)在下图所示的仪器中配制0.1 mol/L的HCl溶液和0.1 mol/L的NaOH溶液肯定不需要的仪器是(填序号)________,配制上述溶液还需要的玻璃仪器是(填仪器名称)_________________________。

(3)配制上述溶液应选用的容量瓶规格是_________(填字母)。
A.50 mL 50 mL B.100 mL 100 mL
C.100 mL 150 mL D.250 mL 250 mL
(4)写出有关的化学方程式______________。
(5)每片胃药中含碳酸钙的质量是____________________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定实验如下:
①需配制0.1 mol?L-1的盐酸和0.1mol?L-1的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol?L-1的氢氧化钠溶液滴定,达到滴定终点时消耗氢氧化钠溶液VmL;
④加入25.00mL0.1mol?L-1的盐酸溶液。
需滴定两次,所需NaOH溶液的体积取平均值,请回答下列问题:
(1)写出实验过程的步骤:___________________(写编号顺序)。
(2)下图所示的仪器中,配制0.1mol?L-1盐酸溶液和0.1mol?L-1氢氧化钠溶液时肯定不需要的仪器是_________(填序号),配制上述溶液还需要的玻璃仪器是_____________________(填仪器名称)。
D.250mL、250mL
(4)写出有关反应的化学方程式:____________。
(5)胃药中含碳酸钙的质量是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1 mol?L-1 的盐酸和0.1mol?L-1 的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol?L-1 的氢氧化钠溶液滴定,需用去VmL达滴定终点;
④加入25.00mL0.1mol?L-1 的盐酸溶液。
(1)写出实验过程的步骤(写编号顺序)______________。
(2)下图所示的仪器中配制0.1mol?L-1 盐酸溶液和0.1mol?L-1 氢氧化钠溶液肯定不需要的仪器是(填序号)_________,配制上述溶液还需要的玻璃仪器是(填仪器名称)__________。

(3)配制上述溶液应选用的容量瓶的规格是(填字母)__________________。
(A)50mL、50mL (B)100mL、100mL
(C)100mL、150mL (D)250mL、250mL
(4)写出有关的化学方程式_____________________________。
(5)胃药中含碳酸钙的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
①配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后加入20 mL蒸馏水;③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,需用去Vx mL达滴定终点;④加入25 mL 0.1 mol·L-1的HCl溶液。
(1)写出全部实验过程的步骤____________(写编写顺序)。

(2)上图所示的仪器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是____________(填序号),配制上述溶液还需用到的玻璃仪器是____________(填仪器名称)。
(3)配制上述溶液应选用的容量瓶规格分别为____________(填字母)。( )
A.50 mL,50 mL B.100 mL,100 mL
C.100 mL,150 mL D.250 mL,250 mL
(4)如果对装有浓盐酸的量筒读数如图读取,配制的稀盐酸的浓度将____________(填“偏高”“偏低”或“无影响”)。如果对容量瓶也如图读取,配制的稀盐酸的浓度将____________(填“偏高”“偏低”或“无影响”)。

(5)写出相关的化学反应方程式:____________________________________________。
(6)胃药中含碳酸钙的质量为:____________ g。(写出计算式并加以文字说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com