
【题目】同温同压下,下列有关等质量的二氧化硫气体和二氧化碳气体的叙述中正确的
A.密度比为16:11 B.密度比为11:16
C.体积比为1:l D.体积比为16:11
【答案】A
【解析】
试题分析:同温同压下,气体摩尔体积相等,二氧化硫和二氧化碳的摩尔质量分别为64g/mol、44g/mol。等质量的二氧化硫和二氧化碳两种气体。A.根据ρ=![]() 知,相同条件下,其密度之比等于其摩尔质量之比,则二氧化硫和二氧化碳的密度之比=64g/mol:44g/mol=16:11,故A正确;B.根据A知,二者的密度之比为16:11,故B错误;C.根据V=
知,相同条件下,其密度之比等于其摩尔质量之比,则二氧化硫和二氧化碳的密度之比=64g/mol:44g/mol=16:11,故A正确;B.根据A知,二者的密度之比为16:11,故B错误;C.根据V=![]() Vm知,相同条件下,等质量的二氧化硫和二氧化碳,其体积之比等于其摩尔质量的反比,所以其体积之比=44g/mol:64g/mol=11:16,故C错误;D.根据C知,二者的体积之比等于11:16,故D错误;故选A。
Vm知,相同条件下,等质量的二氧化硫和二氧化碳,其体积之比等于其摩尔质量的反比,所以其体积之比=44g/mol:64g/mol=11:16,故C错误;D.根据C知,二者的体积之比等于11:16,故D错误;故选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】人体的肌肉细胞中含量最多的物质与过度肥胖者的脂肪细胞中含量最多的物质( )
A. 前者为蛋白质,后者为脂肪 B. 都是水
C. 都是蛋白质 D. 前者是水,后者是脂肪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧显示屏玻璃中含有SiO2、Fe2O3、CeO2、FeO等物质。某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[化学式为xFe2(SO4)3·y(NH4)2SO4·zH2O],流程设计如下:
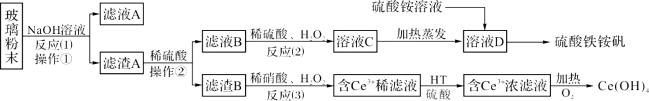
已知:Ⅰ、酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ、CeO2不溶于稀硫酸,也不溶于氢氧化钠溶液。
回答以下问题:
(1)操作①的名称是_____________;该操作所用的玻璃仪器有:烧杯、_________、_________。
(2)反应(2)中过氧化氢的作用是:_________________________。
(3)反应(3)的离子方程式是:_____________________。
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:
2Ce3+(水层)+6HT(有机层)![]() 2CeT3(有机层)+6H+(水层)
2CeT3(有机层)+6H+(水层)
从平衡角度解释:向CeT3(有机层)加入硫酸获得较纯的含Ce3+的水溶液的原因是_________________。
(5)硫酸铁铵矾广泛用于水的净化处理,其净水原理用离子方程式表示为:_________________。
(6)相同物质的量浓度的以下四种溶液中,铵根离子浓度由大到小的顺序是:_________________。
a.xFe2(SO4)3·y(NH4)2SO4·zH2O
b.(NH4)2SO4
c.(NH4)2CO3
d.NH3·H2O
(7)为测定某硫酸铁铵矾样品的组成,现称取14.00 g该样品,将其溶于水配制成100 mL溶液;再将溶液分成两等份,向其中一份加入足量氢氧化钠溶液,过滤、洗涤沉淀、再烘干灼烧至恒重,得到1.60 g固体;向另一份溶液中加入0.5 mol/L硝酸钡溶液100 mL,恰好完全反应。则该硫酸铁铵矾的化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水中含有的水分子数为NA
B.常温常压下,46 g NO2和N2O4的混合气体中含有的氧原子数为2NA
C.1mol/L的Ba(NO3)2溶液中含NO3-离子数为2NA
D.分子数为NA的CO和N2的混合气体的体积约为22.4 L,质量为28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g) ![]() C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
t/s | 0 | 5 | 15 | 25[o] | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速率v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v正<v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于DNA与RNA的叙述,正确的是( )
A. 在细胞内存在的主要部位相同 B. 构成的五碳糖不同
C. 核苷酸之间的连接方式不同 D. 构成的碱基相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示, 该气体所含原子总数为________个,该气体在标准状况下的体积为________L。
(2) 在标准状况下,由CO和CO2组成的混合气体为67.2 L,质量为120 g,此混合物中CO和CO2物质的量之比是________, CO的质量是________,混合气体的平均摩尔质量是 。
(3)若40 g密度为ρ g·cm-3的硝酸钙溶液里含2 g Ca2+,则NO![]() 的物质的量浓度是____________。
的物质的量浓度是____________。
(4)将标准状况下的VL氨气溶于100g水中,得到的氨水密度为ag/cm3,则该溶液的物质的量浓度为 。
(5)标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述:其中正确的是____________
a.体积:②>③>①>④ b.物质的量:②>③>④>①
c.质量:②>③>①>④ d.氢原子个数:①>③>④>②
(6)按体积比为1:2:3所组成的N2、O2、CO2,混合气体20g在标准状况下体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是( )
A.共价化合物中不可能含有离子键
B.H2O比H2S稳定,H—S键比H—O键更难断裂
C.最外层只有一个电子的原子与卤素原子形成的化学键可能是离子键,也可能是共价键
D.离子键和共价键的实质都是电性的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A. 用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B. H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C. 将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D. H3PO2溶于水的电离方程式为H3PO2![]() H++ H2PO2-
H++ H2PO2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com