
| A. | 纯碱溶液和烧碱溶液均呈碱性,说明二者均属于碱 | |
| B. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 | |
| C. | 某酸与Na2CO3反应生成CO2,说明该酸一定是强酸 | |
| D. | 某溶液中滴加KSCN溶液后,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
分析 A、电离出的阴离子全部是氢氧根的化合物为碱;
B、二氧化硫和氯气的漂白原理不同;
C、酸性比碳酸强的酸均能和碳酸钠反应生成二氧化碳;
D、Fe2+和KSCN溶液不显色,而Fe3+和KSCN溶液反应变红色.
解答 解:A、电离出的阴离子全部是氢氧根的化合物为碱,而纯碱是碳酸钠,是盐不是碱,故A错误;
B、二氧化硫和氯气的漂白原理不同,氯气是由于溶于水后有强氧化性而使品红褪色,而二氧化硫是由于和品红反应生成无色物质而使品红褪色,故原理不同,故B错误;
C、酸性比碳酸强的酸均能和碳酸钠反应生成二氧化碳,而醋酸虽然是弱酸,但酸性比碳酸强,故也能和碳酸钠反应生成二氧化碳,故C错误;
D、Fe2+和KSCN溶液不显色,而Fe3+和KSCN溶液反应变红色,故某溶液中滴加KSCN溶液后,溶液不变色,说明溶液中无铁离子,而滴加氯水后,溶液变红色,说明此时溶液中有了铁离子,则此时的铁离子只能是原溶液中本来的Fe2+转化而来的,故溶液中有Fe2+,故D正确.
故选D.
点评 本题考查了碱的概念和常见漂白剂的漂白原理以及离子的检验方法,难度不大,应注意的是氯气和二氧化硫漂白原理的区别.


科目:高中化学 来源: 题型:选择题
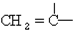 ④-CH3 ⑤
④-CH3 ⑤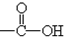 ⑥
⑥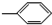
| A. | ④和⑤ | B. | ②③和④ | C. | ①⑤和⑥ | D. | ③和⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有10 个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | CO2的比例模型: | |
| D. | 溴化铵的电子式: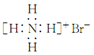 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若向Na2S溶液中通入SO2则产生淡黄色沉淀 | |
| B. | 这三种酸都是二元酸,都能与氢氧化钠反应生成酸式盐和正盐 | |
| C. | 这三种酸的水溶液久置空气中都会变质 | |
| D. | 向氢硫酸、亚硫酸溶液中滴加氯水都会发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 预测的实验现象 | 实验结论或解释 | |
| A | 向饱和Na2CO3 溶液中滴加少量稀盐酸 | 立即有气体逸出 | CO32-+2H+═H2O+CO2↑ |
| B | 将浓硫酸滴加到盛有铜片的试管中,并将 蘸有品红溶液的试纸置于试管口 | 品红试纸褪色 | SO2具有漂白性 |
| C | 铝箔在酒精灯火焰上加热 | 铝熔化但不会滴下 | A12O3的熔点比铝高 |
| D | 向淀粉的酸性水解液中滴入少量新制 Cu (OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙醛与银氨溶液反应:CH3CHO+2[Ag(NH3)2]OH $\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 溴乙烷水解生成乙醇:CH3CH2Br+OH-$→_{△}^{H_{2}O}$CH3CH2OH+Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌是负极,发生还原反应 | |
| B. | O2在正极发生氧化反应 | |
| C. | 工作一段时间后,电解质溶液的碱性会减弱 | |
| D. | 该电池能将化学能全部转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉的能量高于FeS | |
| B. | 铁粉和硫粉的反应常温下不能自发进行 | |
| C. | 该反应是放热反应 | |
| D. | 该反应不会产生污染物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com