
【题目】常温下,下列关于电解质溶液的判断正确的是
A. pH=12的溶液中,K+、Cl-、HCO3-、Na+可以大量共存
B. pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存
C. 0.1 mol·L-1一元酸HA溶液的pH=3,NaA溶液中存在A-+H2O![]() HA+OH-
HA+OH-
D. 0.1 mol·L-1一元碱BOH溶液的pH=10,BOH溶液中存在BOH![]() B++ OH-
B++ OH-
科目:高中化学 来源: 题型:
【题目】某有机物分子式为C4H8,据此推测其结构和性质不可能的是 ( )
A.它与乙烯可能是同系物
B.一氯代物可能只有一种
C.分子结构中甲基的数目可能是0、1、2
D.等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如图(部分反应条件和产物略去)。
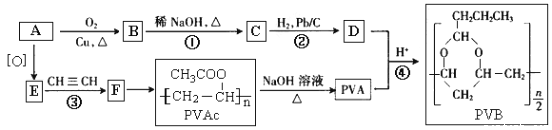
已知:
Ⅰ.A为饱和一元醇,其氧的质量分数约为34.8%
Ⅱ.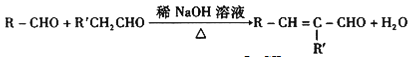
Ⅲ.![]()
请回答:
(1)C中官能团的名称为___________,写出C的反式异构体的结构简式___________,该分子中最多有___________个原子共平面。
(2)D与苯甲醛反应的化学方程式为___________。
(3)③的反应类型是____________________。
(4)PVAc的结构简式为_______________________。
(5)写出与F具有相同官能团的所有同分异构体中的其中二种的结构简式________________________。
(6)参照上述信息,设计合成路线__________________以溴乙烷为原料(其他无机试剂任选)合成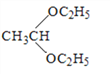
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中能大量共存的一组离子是( )
A.Na+、H+、MnO4-、CO32-
B.NH4+、HCO3-、NO3-、Cl-、
C.Fe3+、NH4+、SCN-、SO42-
D.Na+、ClO-、H+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】60年代美国化学家鲍林提出了一个经验规则:设含氧酸的化学式为HnROm,其中(m-n)为非羟基(-OH)氧原子数,鲍林认为含氧酸的强弱与非羟基氧原子数(m-n)的关系见下表
m-n | 0 | 1 | 2 | 3 |
含氧酸强度 | 弱酸 | 中强 | 强 | 很强 |
实例 | HClO | H3PO4 | HNO3 | HClO4 |
由此判断下列含氧酸酸性最强的是
A. H3AsO4B. H2CrO4C. HMnO4D. H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由乙烯合成乙酸乙酯的几种可能的合成路线。
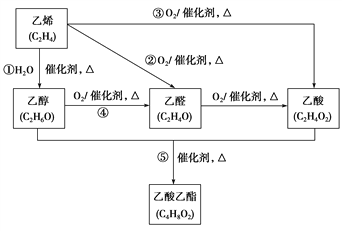
试回答下列问题:
(1)请写出乙酸乙酯的结构简式:________________。
(2)请写出乙酸中官能团的名称:_______________。
(3)写出反应①和反应④的化学方程式:
①______________________________,
④______________________________。
(4)上述几种路线中涉及的有机化学反应基本类型有_________反应、_________反应等(写出两种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生探究如下实验(A):
实验A | 条件 | 现象 |
| 加热 | i.加热后蓝色褪去 ii.冷却过程中,溶液恢复蓝色 ⅲ.一段时间后,蓝色重又褪去 |
(1)使淀粉变蓝的物质是____。
(2)分析现象i、ii认为:在酸性条件下,加热促进淀粉水解,冷却后平衡逆向移动。
设计实验如下,“现象a”证实该分析不合理:
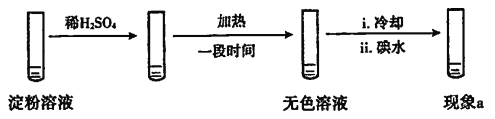
“现象a”是____。
(3)再次分析:加热后单质碘发生了变化,实验如下:
I:取少量碘水,加热至褪色,用淀粉溶液检验挥发出的物质,变蓝。
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷却过程中一直未变蓝;加入稀H2SO4,瞬间变蓝。
对步骤Ⅱ中稀H2SO4的作用,结合离子方程式,提出一种合理的解释:______________。
(4)探究碘水褪色后溶液的成分:
实验1:测得溶液的pH≈5
实验2:取褪色后的溶液,完成如下实验:
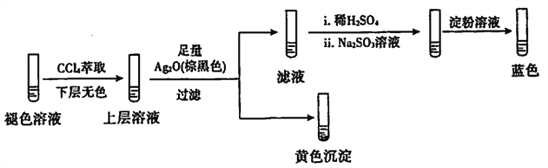
①产生黄色沉淀的离子方程式是____。
②Ag2O的作用是____________。
③依据上述实验,推测滤液中含有的物质(或离子)可能是_________。
(5)结合化学反应速率解释实验A中现象i、现象iii蓝色褪去的原因:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com