
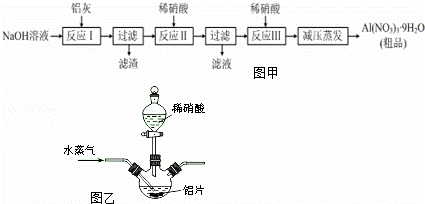
硝铝[Al(NO3)3]是一种常用媒染剂.工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3•9H2O]的流程如图甲:
(1)写出反应Ⅰ的离子方程式: )(任写一个).
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是),可采取的措施为
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是.
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是.
(5)若用图乙所示实验装置制取Al(NO3)3,通入水蒸气的作用是.
考点: 制备实验方案的设计.
分析: 铝灰用氢氧化钠溶液溶解,铝、氧化铝反应生成偏铝酸钠,氧化铁不反应,过滤分离,滤液中含有偏铝酸钠、未反应的NaOH,加入硝酸中和未反应的氢氧化钠,并将偏铝酸钠转化为氢氧化铝沉淀,再过滤分离,氢氧化铝沉淀再用硝酸溶解,得到硝酸铝溶液,经过减压蒸发得到硝酸铝晶体.
(1)反应Ⅰ涉及:铝与氢氧化钠反应生成偏铝酸钠与氢气,氧化铝与氢氧化钠反应生成偏铝酸钠与水;
(2)硝酸属于强酸,可以溶解氢氧化铝沉淀,导致Al元素损失,应控制硝酸用量,可以利用弱酸将偏铝酸根转化为氢氧化铝沉淀而不溶解;
(3)硝酸铝容易发生水解,从抑制硝酸铝水解进行分析解答;
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体,两种气体应是二氧化氮与氧气,二者体积之比为4:1,满足原子守恒与电子转移守恒;
(5)水蒸气温度较高,且可以起搅拌作用,可以加快反应速率.
解答: 解:铝灰用氢氧化钠溶液溶解,铝、氧化铝反应生成偏铝酸钠,氧化铁不反应,过滤分离,滤液中含有偏铝酸钠、未反应的NaOH,加入硝酸中和未反应的氢氧化钠,并将偏铝酸钠转化为氢氧化铝沉淀,再过滤分离,氢氧化铝沉淀再用硝酸溶解,得到硝酸铝溶液,经过减压蒸发得到硝酸铝晶体.
(1)反应Ⅰ涉及:铝与氢氧化钠反应生成偏铝酸钠与氢气,氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应方程式为:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑、Al2O3+2OH﹣=2AlO2﹣+H2O,
故答案为:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑(或Al2O3+2OH﹣=2AlO2﹣+H2O);
(2)硝酸属于强酸,可以溶解氢氧化铝沉淀,导致Al元素损失,需要解决的问题是:如何控制反应终点(或硝酸的用量),可以将加入稀硝酸改为通入过量CO2,避免氢氧化铝沉淀溶解;
故答案为:如何控制反应终点(或硝酸的用量);将加入稀硝酸改为通入过量CO2;
(3)硝酸铝容易发生水解,减压蒸馏可以降低温度、反应Ⅲ中加入的稀硝酸稍过量,都可以抑制硝酸铝水解,
故答案为:抑制硝酸铝水解;
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体,两种气体应是二氧化氮与氧气,二者体积之比为4:1,满足原子守恒与电子转移守恒,反应方程式为:4Al(NO3)3 2Al2O3+12NO2↑+3O2↑,
2Al2O3+12NO2↑+3O2↑,
故答案为:4Al(NO3)3 2Al2O3+12NO2↑+3O2↑;
2Al2O3+12NO2↑+3O2↑;
(5)由于水蒸气温度较高,可以升高反应体系的温度,且可以起搅拌作用,可以加快反应速率,
故答案为:高温度、搅拌,加快反应速率.
点评: 本题考查实验制备方案,侧重考查是对工艺流程的理解、分析与评价,是对学生综合能力的考查,需要学生具备知识的基础与灵活运用的能力,难度中等.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
下列关于化学反应速率的说法,不正确的是()
A. 化学反应速率是衡量化学反应进行快慢程度的物理量
B. 化学反应速率的大小主要取决于反应物的性质
C. 化学反应速率常用单位时间内生成某物质的质量的多少来表示
D. 化学反应速率常用单位有:mol•L﹣1•s﹣1和mol•L﹣1•min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
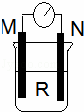
如图所示装置中,M棒变细,N棒变粗.由此判断下表中所列M、N、R物质,其中合理的是()
M N R
A 锌 铜 稀硫酸
B 铜 铁 稀盐酸
C 铁 铜 硝酸银
D 铜 铁 氯化铁
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶 质 HCl NaOH CH3COOH HNO3
溶质的质量分数/% 36.5 40 60 63
物质的量浓度/mol•L﹣1 11.8 14.3 10.6 13.8
这4种溶液中密度最小的是()
A. HCl B. NaOH C. CH3COOH D. HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、HCO3﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()

A. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B. ab段发生的离子反应为:Al3++3OH﹣=Al(OH)3↓,Mg2++2OH﹣=Mg(OH)2↓
C. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D. d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素原子最外层上只有两个电子,该元素()
A. 一定是金属元素
B. 一定是ⅡA族元素
C. 一定是过渡元素
D. 可能是金属元素,也可能不是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中前者属于取代反应,后者属于加成反应的是()
A. 甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液退色
B. 苯与硝酸在一定条件下反应生成硝基苯;乙烯与溴的四氯化碳溶液反应
C. 乙烯与水生成乙醇的反应
D. 在苯中滴入溴水,水层褪色;乙烯与溴水反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com