
在
0℃、1.0×105Pa时,分别向甲、乙、丙三个容器中加入30.0mL同浓度的盐酸,再加入不同质量的同种镁铝合金粉末,得到的有关实验数据列于下表:
求:
(1)盐酸的物质的量浓度;(2)合金中镁的质量分数.
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:
 在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分) 在温度为373K时,将0.400 mol无色的N2O4气体通入4 L抽空
的密闭容器中,立刻出现红棕色,直至建立N2O4 2NO2 的平
衡。右图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,
横坐标为时间)(1)该反应的化学平衡常数表达式为K = 。此温度下,K值= 。
(2)计算在0至20秒时间内,NO2的平均生成速率为 mol•L-1•s-1。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
| T/ K | 323 | 373 |
| K值 | 0.022 | ? |
据此可推测该反应(生成NO2)是 反应(选填“吸热”或“放热”)。
(4)若其他条件不变,反应在373K时达到平衡后,将N2O4和NO2的浓度都增加至0.4mol/L,平衡将向 (填“正”或“逆”)反应方向移动。
(5) 反应在373K时达到平衡时,N2O4的转化率=_________________,若将反应容器的容积缩小为原来的一半,则N2O4的转化率将_________(选填“增大”,“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽怀远县包集中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(14分) 在温度为373K时,将0.400 mol无色的N2O4气体通入4 L抽空
的密闭容器中,立刻出现红棕色,直至建立N2O4  2NO2 的平
2NO2 的平
衡。右图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,
横坐标为时间)(1)该反应的化学平衡常数表达式为K = 。此温度下,K值= 。
(2)计算在0至20秒时间内,NO2的平均生成速率为 mol?L-1?s-1。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
| T/ K | 323 | 373 |
| K值 | 0.022 | ? |
查看答案和解析>>
科目:高中化学 来源:2013届安徽怀远县包集中学高二下学期期中考试化学试卷(解析版) 题型:填空题
(14分) 在温度为373K时,将0.400 mol无色的N2O4气体通入4 L抽空
的密闭容器中,立刻出现红棕色,直至建立N2O4 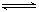 2NO2 的平
2NO2 的平
衡。右图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,
横坐标为时间)(1)该反应的化学平衡常数表达式为K = 。此温度下,K值= 。
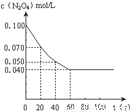
(2)计算在0至20秒时间内,NO2的平均生成速率为 mol•L-1•s-1。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
|
T/ K |
323 |
373 |
|
K值 |
0.022 |
? |
据此可推测该反应(生成NO2)是 反应(选填“吸热”或“放热”)。
(4)若其他条件不变,反应在373K时达到平衡后,将N2O4和NO2的浓度都增加至0.4mol/L,平衡将向 (填“正”或“逆”)反应方向移动。
(5) 反应在373K时达到平衡时,N2O4的转化率=_________________,若将反应容器的容积缩小为原来的一半,则N2O4的转化率将_________(选填“增大”,“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com