
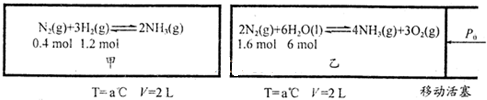
| c2(NH3) |
| c(N2)?c3(H2) |
| 0.22 |
| 0.1×0.33 |
| 400 |
| 27 |
| 1.2 |
| 1.6 |
| 3 |
| 4 |
| 400 |
| 27 |
| 3 |
| 4 |
| c3(O2)×c4(NH3) |
| c2(N2)×c6(H2O) |
| 0.33×0.44 |
| 1.42×5.46 |
| 0.2 |
| 1.6 |


科目:高中化学 来源: 题型:
A、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH3)
| ||||||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||||||
| C、向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→ 2C6H5OH+2CO32- | ||||||
| D、甘氨酸(H2N-CH2-COOH)与氢氧化钠溶液反应:H2N-CH2-COOH+OH-→H2N-CH2COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、
| ||||
C、
| ||||
| D、锎元素的相对原子质量为252 |
查看答案和解析>>
科目:高中化学 来源: 题型:
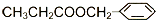 )在食品、药品、化妆品等方面应用广泛,用烷烃A合成香精及其他两种有机物的路线如下:
)在食品、药品、化妆品等方面应用广泛,用烷烃A合成香精及其他两种有机物的路线如下: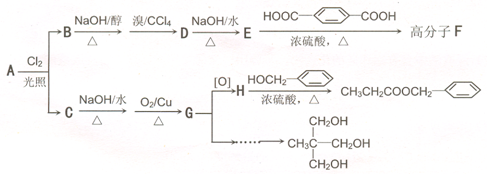

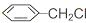
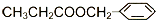 互为同分异构体的是:
互为同分异构体的是: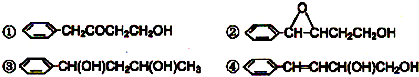
 直接合成该香精,化学方程式为
直接合成该香精,化学方程式为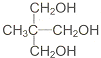 ,写出合成路线(注明条件,不要求写化学方程式)
,写出合成路线(注明条件,不要求写化学方程式)查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.10mL | 18.60mL |
| 第二次 | 0.30mL | 18.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
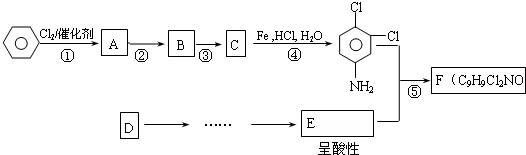
| NaCN |
| H2O |
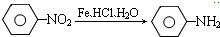
查看答案和解析>>
科目:高中化学 来源: 题型:
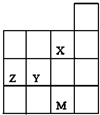
| A、Y、Z的最高价氧化物的水化物酸性为Y<Z |
| B、M的最外层电子数比Z大10 |
| C、X、M的气态氢化物的稳定性M>X |
| D、X、Y形成简单离子的最外层电子均满足8e-稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
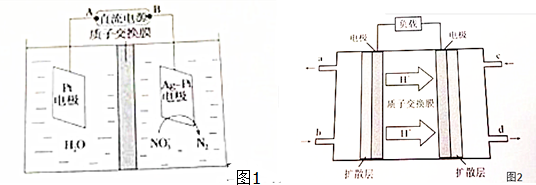
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于20mL |
| B、小于20mL |
| C、等于30mL |
| D、大于30ml. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com