
| A. | 等浓度的碳酸钠、碳酸氢钠溶液混合后:c(CO32-)<c(HCO3-) | |
| B. | 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 | |
| C. | 在恒温、恒容条件下,SO2与O2按照物质的量之比为2:1通入达到平衡,若向上述平衡体系中通入氧气,则SO3的百分含量将减小 | |
| D. | pH=3的盐酸和醋酸,等体积混合因为醋酸被稀释pH>3 |
分析 A.碳酸根离子水解程度大于碳酸根离子;
B.溶液中电荷的浓度不变;
C.通入氧气,混合物的总物质的量增大;
D.根据醋酸的电离常数分析.
解答 解:A.碳酸根离子水解程度大于碳酸根离子,溶液中c(HCO3-)较大,则c(CO32-)<c(HCO3-),故A正确;
B.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,溶液中电荷的浓度不变,所以导电能力不变,故B错误;
C.在恒温、恒容条件下,SO2与O2按照物质的量之比为2:1通入达到平衡,若向上述平衡体系中通入氧气,平衡正向移动,SO3的物质的量大,但是混合物的总物质的量增大程度更大,所以SO3的百分含量将减小,故C正确;
D.pH=3的盐酸和醋酸,等体积混合,c(CH3COOH)和c(CH3COO-)同时减小,Ka=$\frac{c(C{H}_{3}CO{O}^{-})×c({H}^{+})}{c(C{H}_{3}COOH)}$不变,所以氢离子浓度不变,pH不变,故D错误.
故选AC.
点评 本题考查了盐的水解和弱电解质的电离,题目难度中等,注意把握溶液中离子浓度大小比较方法以及决定溶液导电性的因素,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A>B>C>D | B. | 离子半径:C>D>B>A | ||
| C. | 原子序数:d>c>b>a | D. | 最外层电子数:D>C>B>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在金属区、非金属区交界线上,寻找具有半导体性能的材料 | |
| B. | 形成化合物种类最多的元素在第14列 | |
| C. | 第ⅡA族的右边是第ⅢB族,第ⅢA族的左边是第ⅡB族 | |
| D. | 某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m-nR或RH2m-n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑦⑧⑨ | B. | ③⑤⑥⑦⑧⑨ | C. | ②③④⑤⑦⑧ | D. | ①②④⑥⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 C2H2 | B. | C2H6 C3H6 | C. | C2H4 C3H6 | D. | C2H4 C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
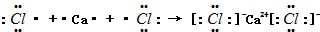 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L 氢氰酸溶液的pH约为3 | |
| B. | 1mol/L 氢氰酸钠溶液的pH约为8.5 | |
| C. | 10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 | |
| D. | 在相同条件下,HCN溶液的导电性比氢氟酸溶液的弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com