
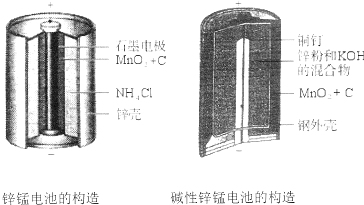
| A£® | øƵē³Ų·“Ó¦ÖŠ¶žŃõ»ÆĆĢĘš“ß»Æ×÷ÓĆ | |
| B£® | µē³Ųøŗ¼«·“Ó¦Ź½ĪŖ£ŗ2MnO2+2e-+2H2OØT2MnOOH+2OH- | |
| C£® | µ±0.1molZnĶźČ«·“Ó¦Ź±£¬Į÷¾µē³ŲÄŚ²æµÄµē×ÓøöŹżĪŖ1.204”Į1023 | |
| D£® | ¼īŠŌŠæĆĢµē³ŲÓĆŠæ·ŪĢę“śĮĖŌŠæĆĢµē³ŲµÄŠææĒ£¬Ōö“óĮĖ·“Ó¦ĪļµÄ½Ó“„Ć껿£¬¼ÓæģĮĖ·“Ó¦ĖŁĀŹ£¬¹Ź·ÅµēµēĮ÷“ó |
·ÖĪö Óɵē³Ų×Ü·“Ó¦Zn+2MnO2Ź®H2O=ZnO+2MnO£ØOH£©æÉÖŖ£¬Zn±»Ńõ»Æ£¬ĪŖŌµē³ŲµÄøŗ¼«£¬µē¼«·“Ó¦ĪŖZn-2e-+2OH-=ZnO+H2O£»MnO2±»»¹Ō£¬ĪŖŌµē³ŲÕż¼«£¬µē¼«·“Ó¦ĪŖMnO2+H2O+e-=MnO£ØOH£©+OH-£¬ÓÉ“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®øƵē³Ų·“Ó¦ÖŠ¶žŃõ»ÆĆĢŹĒŃõ»Æ¼Į£¬²»ŹĒ“߻ƼĮ£¬¹ŹA“ķĪó£»
B£®øĆŌµē³ŲÖŠÕż¼«ÉĻµĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ2MnO2+2H2O+2e-=2MnOOH+2OH-£¬¹ŹB“ķĪó£»
C£®¹¤×÷ÖŠ£¬øŗ¼«·“Ó¦ĪŖZn-2e-+2OH-ØTZn£ØOH£©2£¬ĶāµēĀ·ÖŠĆæĶعżO.1molµē×Ó£¬ĻūŗĵÄZnµÄĪļÖŹµÄĮæĪŖ0.1mol£¬Į÷¾µē³ŲĶāµēĀ·µÄµē×ÓøöŹżĪŖ1.204”Į1023£¬¹ŹC“ķĪó£»
D£®Šæ·ŪĢę“śĮĖŌŠæĆĢµē³ŲµÄŠææĒ£¬Ōö“óĮĖ·“Ó¦ĪļµÄ½Ó“„Ć껿£¬¼ÓæģĮĖ·“Ó¦ĖŁĀŹ£¬¹Ź·ÅµēµēĮ÷“󣬹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧµēŌ“µÄ¹¤×÷ŌĄķ£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņāµē¼«·“Ó¦·½³ĢŹ½µÄŹéŠ“ŗĶÅŠ¶Ļ£®


 ĆūŹ¦µ¼ŗ½µ„ŌŖĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
ĆūŹ¦µ¼ŗ½µ„ŌŖĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
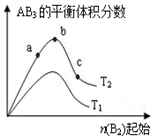 ij»ÆѧæĘŃŠŠ”×éŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäijŅ»Ģõ¼ž¶ŌA2£Øg£©+3B2£Øg£©?2AB3£Øg£©»ÆŃ§Ę½ŗāדĢ¬µÄÓ°Ļģ£¬µĆµ½ČēĶ¼ĖłŹ¾µÄ±ä»Æ¹ęĀÉ£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£¬øł¾ŻČēĶ¼ÅŠ¶Ļ£ŗ
ij»ÆѧæĘŃŠŠ”×éŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäijŅ»Ģõ¼ž¶ŌA2£Øg£©+3B2£Øg£©?2AB3£Øg£©»ÆŃ§Ę½ŗāדĢ¬µÄÓ°Ļģ£¬µĆµ½ČēĶ¼ĖłŹ¾µÄ±ä»Æ¹ęĀÉ£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£¬øł¾ŻČēĶ¼ÅŠ¶Ļ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢ŁµÄ²śĪļ±Č¢ŚµÄ²śĪļĪČ¶Ø | |
| B£® | I2£Øs£©=I2£Øg£©”÷H=+17.00KJ•mol-1 | |
| C£® | ¢ŚµÄ·“Ó¦Īļ×ÜÄÜĮæ±Č¢ŁµÄ·“Ó¦Īļ×ÜÄÜĮæµĶ | |
| D£® | 1molI2£Øg£©ÖŠĶØČė1molH2£Øg£©£¬·¢Éś·“Ó¦Ź±·ÅČČ9.48KJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ģå»ż£ŗ¢Ś£¾¢Ū | B£® | ĆÜ¶Č£ŗ¢Ü£¾¢Ł | C£® | ÖŹĮæ£ŗ¢Ū£¾¢Ł | D£® | ĒāŌ×ÓøöŹż£ŗ¢Ł£¾¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2ŗĶO2·“Ӧɜ³ÉĖ® | B£® | CuOĶ¶ČėĻ”ĮņĖįÖŠ | ||
| C£® | øßĪĀģŃÉÕŹÆ»ŅŹÆÖĘCO2 | D£® | NaOHČÜŅŗŗĶK2SO4ČÜŅŗ»ģŗĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
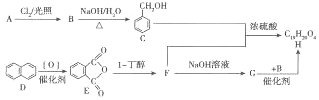
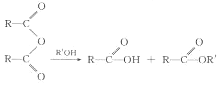 ¢Ś·“Ó¦F”śG½ö·¢ÉśÖŠŗĶ·“Ó¦
¢Ś·“Ó¦F”śG½ö·¢ÉśÖŠŗĶ·“Ó¦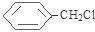 +NaOH$”ś_{”÷}^{H_{2}O}$
+NaOH$”ś_{”÷}^{H_{2}O}$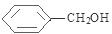 +NaCl£®
+NaCl£®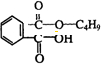 £®
£®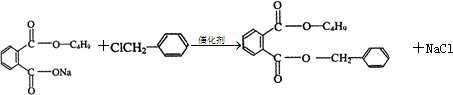 £®
£®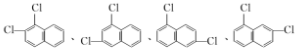 ÖŠČĪŅ»Ö֣؊“³öŅ»ÖÖ¼“æÉ£©£®
ÖŠČĪŅ»Ö֣؊“³öŅ»ÖÖ¼“æÉ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×ÓŅ׊Ī³É-2¼ŪŅõĄė×Ó | |
| B£® | µ„ÖŹ¾łĪŖĖ«Ō×Ó·Ö×Ó£¬¾ßÓŠŃõ»ÆŠŌ | |
| C£® | Ō×Ó°ė¾¶ĖęŌ×ÓŠņŹżµŻŌöÖš½„¼õŠ” | |
| D£® | Ēā»ÆĪļµÄĪČ¶ØŠŌĖęŌ×ÓŠņŹżµŻŌöŅĄ“ĪŌöĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦ĖŁĀŹÓĆÓŚŗāĮæ»Æѧ·“Ó¦½ųŠŠµÄæģĀż | |
| B£® | ¾ö¶Ø·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ·“Ó¦ĪļµÄŠŌÖŹ | |
| C£® | ·“Ó¦ĖŁĀŹŌ½“󣬷“Ó¦ĻÖĻó¾ĶŅ»¶ØŌ½Ć÷ĻŌ | |
| D£® | Ōö“ó·“Ó¦ĪļµÄÅØ¶Č”¢Ģįøß·“Ó¦ĪĀ¶Č¶¼ÄÜŌö“ó·“Ó¦ĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com