
【题目】亚硝酸钠外观与食盐相似,有咸味,误食会引起中毒,致死量 0.3g~0.5g.工业用盐中含有亚硝酸钠.已知 NaNO2能发生如下反应:
NO ![]() +I﹣+H+=NO+I2+H2O 请回答下列问题
+I﹣+H+=NO+I2+H2O 请回答下列问题
(1)配平上面离子方程式(在“”上填上系数)
(2)某工厂废液中含有 3%~5%的NaNO2 , 直接排放会造成水体污染,加入下列物质 中的某一种就能使 NaNO2转化为不引起污染的 N2 , 该物质是
A.NaCl B.H2SO4 C.NH4Cl D.H2O2
发生反应的离子方程式为 .
(3)在反应 2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O中,若生成 71gCl2 , 则被氧化的 HCl 的质量是 g,转移的电子数是 .
【答案】
(1)
2,2,4,2,1,2
(2)C;NO ![]() +NH
+NH ![]() =N2+2H2O
=N2+2H2O
(3)73;2NA
【解析】解:(1)反应中亚硝酸根离子氮元素化合价变化:+3→+2,碘离子中碘元素化合价变化:﹣1→0,要使化合价升降数目相等,则亚硝酸根离子系数为2,碘离子系数为2,依据原子个数守恒,反应的方程式:2NO ![]() +2I﹣+4H+=2NO+I2+2H2O;所以答案是:2;2;4;2;1;2;
+2I﹣+4H+=2NO+I2+2H2O;所以答案是:2;2;4;2;1;2;
(2)因NaNO2转化为不引起污染的N2的过程中N的化合价降低,另一物质化合价必升高,物质具有还原性,只有NH4Cl符合,亚硝酸根离子与铵根离子发生归中反应生成氮气和水,离子方程式:NO ![]() +NH4+=N2+2H2O;所以答案是:C;NO
+NH4+=N2+2H2O;所以答案是:C;NO ![]() +NH
+NH ![]() =N2+2H2O;
=N2+2H2O;
(3)依据方程式可知2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O中,有16mol氯化氢参加反应,其中有10mol氯化氢中﹣1价的氯元素化合价升高被氧化生成氯气,所以每生成5mol氯气被氧化的氯化氢的物质的量为10mol,转移10mol电子,则若生成 71gCl2 , 其物质的量为1mol,则被氧化的氯化氢的物质的量为2mol,质量m=2mol×36.5g/mol=73g;转移电子数目为2mol,个数为2NA;所以答案是:73; 2NA(或 1.204×1024).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维。它的一种单体芥子醉结构简式如下图所示,下列有关芥子醇的说法正确的是( )

A. 芥子醉分子式为C11H10O4属于芳香化合物
B. 芥子醇分子中所有碳原子不可能在同一平面上
C. 1 mol芥子醉与足量浓溴水反应,最多消耗3 mol Br2
D. 芥子醉能发生的反应类型有氧化、取代、加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A-F是几种典型有机代表物的分子模型。请看图回答下列问题·
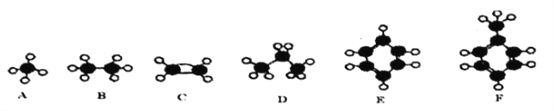
(1)A的二氯取代物有_____(填数字)种:
(2)能够发生加成反应的烃有____(填数字)种:
(3)常温下含碳量最高的气态烃是______(填字母):
(4)一卤代物种类最多的是_____((填字母);
(5)写出实验室制取C的化学方程式______________________________________;
(6)写出E发生溴代反应的化学方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是


![]()

图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A. 图I所示装置用于Cu和浓H2SO4制取少量的SO2气体
B. 图Ⅱ装置可验证非金属性:Cl>C>Si
C. 图Ⅲ可用于收集气体H2、CO2、Cl2、NH3
D. 图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。据此判断下列说法中正确的是( )

A. 由图1知,石墨转变为金刚石是吸热反应
B. 由图2知,S(g)+O2(g)===SO2(g) ΔH1,S(s)+O2(g)===SO2(g) ΔH2,则ΔH1>ΔH2
C. 由图3知,白磷比红磷稳定
D. 由图4知,CO(g)+H2O(g)===CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一定量饱和 Ca(OH)2溶液中通入二氧化碳气体后,产生 CaCO3 白色沉淀的质量与二氧化碳体积之间的关系曲线.
试回答:OA 段所表示的反应离子方程式是: ,
AB 段所表示的反应化学方程式是: ,
将 B 处生成的溶液煮沸,可见到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g)![]() 3Z(g) H=﹣a kJ·molˉ1(a>0),下列说法不正确的是
3Z(g) H=﹣a kJ·molˉ1(a>0),下列说法不正确的是
A. 0.1 mol X和0.2 mol Y充分反应生成Z,放出能量一定小于0.1 a kJ
B. Y的起始浓度不能为零,平衡浓度也不能为零
C. 在其他条件不变的情况下,降低反应温度,正、逆反应速率均减小
D. 当反应达到平衡状态时,一定存在3v(Y)正=2v(Z)逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com