
| A. | 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 | |
| B. | 实验室从海带提取碘单质的步骤是:取样、灼烧、溶解、过滤、萃取 | |
| C. | 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 | |
| D. | 中和滴定实验中,如用于盛放待测液的锥形瓶洗净后未经干燥,不影响测定结果 |
分析 A.用乙醇和浓硫酸加热制备乙烯时,加热温度为170℃;
B.海带中没有单质碘,存在碘离子,需要将碘离子转化为碘再萃取;
C.金属汞一旦洒落在实验室地面或桌面,加硫磺粉处理;
D.锥形瓶是否干燥不影响待测液的溶质的物质的量.
解答 解:A.用乙醇和浓硫酸加热制备乙烯时,加热温度为170℃,水浴加热时温度不超过100℃,故A错误;
B.海带中没有单质碘,存在碘离子,需要将碘离子转化为碘再萃取,所以其操作步骤是取样、灼烧、溶解、过滤、氧化、萃取,故B错误;
C.金属汞一旦洒落在实验室地面或桌面,加硫磺粉处理,且金属汞不能深埋处理,易污染土壤和地下水,故C错误;
D.锥形瓶是否干燥不影响待测液的溶质的物质的量,无需干燥,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及实验操作、实验安全等知识点,明确实验原理、物质性质、实验操作规范是解本题关键,注意从实验操作规范性和实验评价性分析解答,易错选项是BD.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{a(A-N+3)}{A+3}$ | B. | $\frac{a(A-N+8)}{A+16}mol$ | ||
| C. | $\frac{a(2A-2N+40)}{2A+90}$ | D. | $\frac{2A-2N+24}{2A+54}mol$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
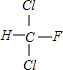 ;
;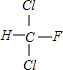 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$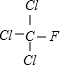 +HCl,生成氟氯昂可表示为F-11.
+HCl,生成氟氯昂可表示为F-11.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
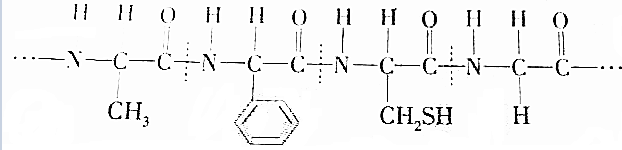
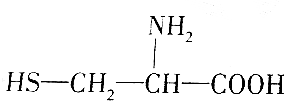 (半胱氨酸)
(半胱氨酸)| A. | ①②③ | B. | ②③④ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:己烷>2-甲基丁烷>戊烷 | B. | 同分异构体种类:戊烷<戊烯 | ||
| C. | 密度:苯<水<1,1,2,2-四溴乙烷 | D. | 点燃时火焰明亮程度:乙烯>乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com