
| A. | 肯定有SO2和NO或NO2中的至少一种 | B. | 肯定只有NO | ||
| C. | 可能有Cl2和O2 | D. | 肯定没有Cl2、O2和NO2 |
分析 由于气体呈无色,所以其中一定没有Cl2、NO2,气体通过品红,品红褪色,说明混合气体中含有SO2,剩余气体排入空气中呈红棕色,说明其中含有NO,结合原混合气体无色,说明混合气体中没有O2.
解答 解:某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体,该气体是无色的,则一定不能含有氯气(黄绿色)和NO2(红棕色).混合气体通过品红溶液后,品红溶液褪色,说明含有SO2.把剩余气体排入空气中,很快变为红棕色,这说明含有NO,因此就一定不能含有O2,原混合气体成分肯定没有Cl2、O2和NO2,
故选D.
点评 本题需要注意的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 气体的平均分子量不再变化 | B. | 反应的平衡常数不变 | ||
| C. | ?(H2)=2 ?(HI) | D. | 气体的颜色不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度相同的硫酸氢铵溶液和醋酸铵溶液中,硫酸氢铵中的铵根离子物质的量浓度较小 | |
| B. | 在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)<Ksp(AgCl) | |
| C. | 物质的量浓度均为0.02 mol/L的弱酸HX及其盐NaX等体积混合后:c(X-)+c(HX)=0.02 mol/L | |
| D. | 己知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.在含C1-、CrO42-浓度相同的溶液中滴加AgNO3溶液时,首先生成Ag2CrO4沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000mL,106g | B. | 1000mL,286g | C. | 950mL,100.7g | D. | 950mL,271.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
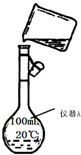 化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合右侧下列实验装置图回答有关问题:
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合右侧下列实验装置图回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是化学反应进行快慢程度的物理量 | |
| B. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 | |
| C. | 在同一个反应中,可以用反应物或生成物来表示反应速率 | |
| D. | 化学反应速率的常用单位有mol/(L•s)和mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
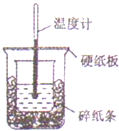 50ml0.5mol•L-1盐酸与50ml•L-1NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是( )
50ml0.5mol•L-1盐酸与50ml•L-1NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是( )| A. | 从实验装置上看,除了缺少环形玻璃搅拌棒外没有其他问题 | |
| B. | 大烧杯上如不盖硬纸板,测得的中和热数值会偏大 | |
| C. | 用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会偏大 | |
| D. | 实验中改用60ml0.5mol•L-1盐酸跟50ml0.55mol•L-1NaOH溶液进行反应,与上实验相比,所放出的热量不相等,但是所求中和热相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 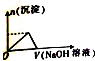 | B. | 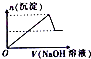 | C. | 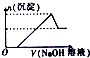 | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com