
| A. | 32 | B. | 32 g•mol-1 | C. | 64 g•mol-1 | D. | 64 |
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:解答题
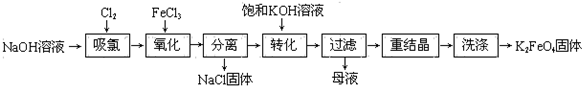
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发的过程中,用酒精灯一直加热到全部固体析出 | |
| B. | 过滤时,为了加快过滤速率,可用玻璃棒在过滤器内搅拌 | |
| C. | 对医用酒精进行蒸馏操作可得到更高纯度的酒精溶液 | |
| D. | 分液漏斗盛装的是液体,振荡后不必扭开旋塞把气体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2X -+Z2=X2+2Z -; | B. | 2R-+Z2=R2+2Z - | ||
| C. | 2R-+Y2=R2+2Y - | D. | 2Z -+Y2=Z2+2Y - |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色;有气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液出现血红色 |
| ③ | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、NO${\;}_{3}^{-}$、Na+ | |
| B. | 在能使石蕊变红色的溶液中:Na+、S2-、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | |
| C. | 在加入铝粉能产生H2的溶液中:NH${\;}_{4}^{+}$、Na+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 常温下由水电离出的c(H+)=1×10-12 mol•L-1的溶液中:K+、Cl-、NO${\;}_{3}^{-}$、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com