
| x |
| 2 |
| 3x |
| 2 |
| x |
| 2 |
| 3x |
| 2 |
| 3x |
| 2 |
| ��c |
| t |
| 0.8mol/L |
| 5min |
| c3(C) |
| c2(A)?c(B) |
| 1.23 |
| 1.22?0.6 |
| 0.4 |
| 1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
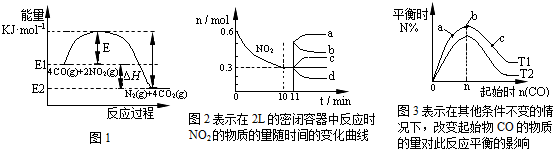
| A����һ���¶ȡ��̶��ݻ����ܱ���������������ܶȲ��ٸı����˵���������淴Ӧ�Ѵ�ƽ�� | B����ͼ1�ɵü����ʵ��Ĵ�����E�͡�H����С | C��ͼ2��0��10min�ڸ÷�Ӧ��ƽ������v��CO��=0.03mol?L-1?min-1����11min�������������䣬ѹ�����������Ϊ1L����n��NO2���ı仯����Ϊd | D��ͼ3��T1��T2��ʾ�¶ȣ���Ӧ�¶��µ�ƽ�ⳣ��ΪK1��K2����T1��T2��K1��K2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ���и�һ��ѧ�������ʼ����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£����ݻ�Ϊ1 L���ܱ������м���1 mol A�����2 mol B���壬������Ӧ��A(g)��2B(g) 2C(g)�����������˵���÷�Ӧ�ﵽƽ��״̬���ǣ� ��
2C(g)�����������˵���÷�Ӧ�ﵽƽ��״̬���ǣ� ��
A��������A��B��C��Ũ��֮��Ϊ1��2��2
B����λʱ������0.1 mol��L��1 A��ͬʱ����0.2 mol��L��1 B
C��������ѹǿ����ʱ��仯
D��������ƽ����Է�����������ʱ��仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��09-10�꽭����У��һ��ѧ������������ѧ�� ���ͣ�ѡ����
��һ���¶��£����ݻ�Ϊ1 L���ܱ������м���1 mol
A�����2 mol B���壬������Ӧ��A(g)
+ 2B(g)  2C(g)������˵�����ڸ÷�Ӧ�ﵽƽ���־���ǣ� ��
2C(g)������˵�����ڸ÷�Ӧ�ﵽƽ���־���ǣ� ��
A��������A��B��C��Ũ��֮��Ϊ1:2:2
B����λʱ������0.1 mol / L Aͬʱ����0.2 mol / L C
C��������ѹǿ����ʱ��仯
D�������������ƽ����Է�����������ʱ��仯
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com