
完成下列转化关系中标号反应的化学方程式,并指出反应类型。

①______________________________,________________________________________;
②______________________________,________________________________________;
③______________________________,_________________________________________;
④______________________________,__________________________________________;
⑤______________________________,_________________________________________;
⑥______________________________,_________________________________________。
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
除去乙酸乙酯中的乙酸杂质,下列方法可行的是( )
A.加乙醇、浓硫酸,加热
B.加NaOH溶液,充分振荡后,分液
C.直接分液
D.加饱和Na2CO3溶液,充分振荡后分液
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.1 mol的镁和铝的混合物溶于100 mL 2 mol·L-1H2SO4溶液中,然后再滴加1 mol·L-1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示:
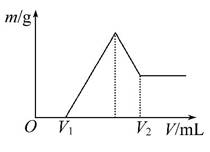
①有关反应的离子方程式为 ______________________________________。
②当V1=160 mL时,则金属粉末中n(Mg)=_________mol,V2=________mL。
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
 的同分异构体中含有苯环的还有________种(不考虑立体异构),其中核磁共振氢谱为4组峰,且面积比为6∶2∶2∶1的是________________________(写出其中一种的结构简式)。
的同分异构体中含有苯环的还有________种(不考虑立体异构),其中核磁共振氢谱为4组峰,且面积比为6∶2∶2∶1的是________________________(写出其中一种的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料。甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料。下列说法中错误的是( )

A.甲物质可以在引发剂作用下生成有机高分子化合物
B.1 mol乙物质可与2 mol钠完全反应生成1 mol氢气
C.丙物质能使酸性高锰酸钾溶液褪色
D.甲、乙、丙三种物质都可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有机合成片段
现有下列转化:

(1)写出A与浓溴水反应的化学方程式____________。
(2)A→B→C转化的反应类型分别是________________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示为一个有机合成反应的流程图:

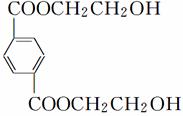
请根据图示回答下列问题:
(1)写出中间产物A、B、D的结构简式。
A______________________,B________________________________________________________________________,
D________________。
(2)在图中①至⑦的反应中属于取代反应的是________。(填序号)
(3)写出C的同分异构体X,要求符合以下两个条件:
ⅰ.苯环上有两个侧链;
ⅱ.1 mol X与足量NaHCO3溶液反应产生1 mol CO2气体。
写出符合上述两条件的X的所有结构简式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为2Zn+O2===2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是( )
A.锌为正极,空气进入负极反应
B.负极反应为Zn+2OH-—→ZnO+H2O+2e-
C.正极发生氧化反应
D.电解液可以是强酸也可以是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
H2NOONH4(s) 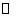 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
| 温度( | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度( | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
氨基甲酸铵分解反应的焓变 H__________0(填“>”、“<”或“=”)
H__________0(填“>”、“<”或“=”)
可以判断该分解反应已经达到化学平衡的是____________.(填字母)
A. 2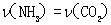
B. 密闭容器中总压强不变
C. 密闭容器中混合气体的密度不变
D. 密闭容器中氨气的体积分数不变
根据表中数据,计算25.0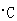 时的分解平衡常数为____________.
时的分解平衡常数为____________.
(2) 25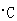 时,NH3·H2O电离常数Kb=1.8
时,NH3·H2O电离常数Kb=1.8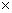 10-5,Mg(OH)2的溶度积常数Ksp=1.8
10-5,Mg(OH)2的溶度积常数Ksp=1.8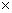 10-11,计算0.5mol/L氨水的pH约为__________.(已知lg3
10-11,计算0.5mol/L氨水的pH约为__________.(已知lg3 0.5)
0.5)
在某氯化镁溶液中加入一定量的某浓度的氨水后,测得混合液PH=11,则此温度下残留在溶液中的c(Mg2+)=_________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com