
 C(g)+D(g)已达到平衡状态的现象是
C(g)+D(g)已达到平衡状态的现象是 | A.混合气体的压强 | B.混合气体的密度 |
| C.气体的总物质的量 | D.单位时间内生成n mol C的同时消耗2n molB |
科目:高中化学 来源:不详 题型:单选题
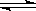 2NH3已达到平衡状态 ( )
2NH3已达到平衡状态 ( ) | A.1个N≡N键断裂的同时,有6个H—H键断裂 |
| B.1个N≡N键断裂的同时,有3个H—H键断裂 |
| C.1个N≡N键断裂的同时,有6个N—H键断裂 |
| D.1个N≡N键断裂的同时,有6个N—H键形成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
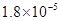 ,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=
,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=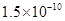
 mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:

 mol·L-1HF溶液与
mol·L-1HF溶液与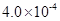 mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。
mol·L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化), (填“有”或“无”)沉淀产生。| A.NH4Cl | B.NH4SCN? | C.CH3COONH4 | D.NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2O(g) + CO(g),反应所处的温度相同,但起始浓度不同,其中 甲:n(CO2)=n(H2)=1 mol;乙:n(CO2)=1 mol, n(H2)=2mol;丙:n(CO2)=n(H2)=1mol n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是( )
H2O(g) + CO(g),反应所处的温度相同,但起始浓度不同,其中 甲:n(CO2)=n(H2)=1 mol;乙:n(CO2)=1 mol, n(H2)=2mol;丙:n(CO2)=n(H2)=1mol n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是( )| A.乙>甲>丙 | B.甲>丙>乙 | C.乙>丙>甲 | D.甲>乙>丙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )
2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表: ( )| 容器 | 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(>0) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26
Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 A2(g)+B2(g)达到平衡状态的标志是 ( )
A2(g)+B2(g)达到平衡状态的标志是 ( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
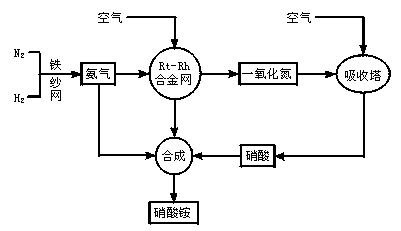
 2NH3(g),Q>0。请解释:
2NH3(g),Q>0。请解释:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com