

| △c |
| △t |
| 1 |
| 2 |
| △c |
| △t |
| 0.9mol/L |
| 6min |
| 0.9 |
| 0.3×0.1 |
| (0.9+0.5)mol/L |
| (0.3+0.5)mol/L×(0.1+0.5)mol/L |


科目:高中化学 来源: 题型:


 是没食子酸的球棍模型,请结合有机结构特征,写出没食子酸的结构简式
是没食子酸的球棍模型,请结合有机结构特征,写出没食子酸的结构简式| NH2-NH2 |
| 水解 |
| 氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
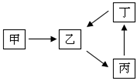 甲、乙、丙、丁四种物质转化关系如右图.已知甲是一种导致钢铁生锈及许多还原性物质变质的单质,化合物乙、丙、丁均含有第三周期一种相同元素R.
甲、乙、丙、丁四种物质转化关系如右图.已知甲是一种导致钢铁生锈及许多还原性物质变质的单质,化合物乙、丙、丁均含有第三周期一种相同元素R.查看答案和解析>>
科目:高中化学 来源: 题型:
 使用锂离子电池为动力汽车,可减少有害气体的排放.锰酸锂离子蓄电池的反应式为:Li1-xMnO4+LixC
使用锂离子电池为动力汽车,可减少有害气体的排放.锰酸锂离子蓄电池的反应式为:Li1-xMnO4+LixC| 放电 |
| 充电 |
| A、充电时电池内部Li+向正极移动 |
| B、放电过程中,电能转化为化学能 |
| C、放电时电池的正极反应式为:Li1-xMnO4+xe-+xLi+=LiMnO4 |
| D、充电时电池的正极应与外接电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol水的摩尔质量为1.8 g/mol | ||
| B、1 molH2O的质量等于NA个H2O质量的总和 | ||
C、一个12C原子的真实质量为
| ||
| D、1 mol任何物质的质量以克为单位等于该物质的化学式式量 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、实验室在蒸发皿中灼烧干海带,并且用玻璃搅拌 |
| B、含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应 |
| C、在碘水中加入几滴淀粉溶液,溶液变蓝色 |
| D、碘水中加入CCl4得到I2的CCl4的溶液,该操作为“萃取” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③④⑤ |
| C、①②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgSO4溶液:c(Mg2+)+c(H+)=c (SO42-)+c(OH-) |
| B、将0.2mol?L-1CH3COOH溶液与0.1mo1?L-1NaOH溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C、将pH=2的盐酸与0.01 mo1?L-1氨水等体积混合:c(NH4+)=c (Cl-) |
| D、由AgCl和AgI固体混合物与水形成的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com