
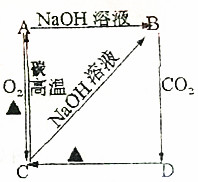
 根据如图所示变化关系,请回答下列问题.
根据如图所示变化关系,请回答下列问题.分析 由题给信息以及转化关系可知C为氧化物,且在高温下可与碳反应生成A,A能与氢氧化钠溶液反应,只有Si符合,即A应为Si,则C为SiO2,B为Na2SiO3,D为H2SiO3,结合对应物质的性质解答该题.
解答 解:由题给信息以及转化关系可知C为氧化物,且在高温下可与碳反应生成A,A能与氢氧化钠溶液反应,只有Si符合,即A应为Si,则C为SiO2,B为Na2SiO3,D为H2SiO3,
(1)由以上分析可知A为Si,B为Na2SiO3,C为SiO2,D为H2SiO3,故答案为:Si;Na2SiO3;SiO2;H2SiO3;
(2)C为SiO2,在高温下可与碳反应生成A,反应的方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO,故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO;
(3)Si与氢氧化钠反应生成硅酸钠和氢气,反应的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑,二氧化硅与氢氧化钠反应生成硅酸钠和水,反应的离子方程式为SiO2+2OH-=SiO32-+H2O,故答案为:Si+2OH-+H2O=SiO32-+2H2↑;SiO2+2OH-=SiO32-+H2O.
点评 本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意把握硅及其化合物的性质以及转化关系,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 对于可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时C的百分含量与温度(T)和压强(P)关系如图所示,下面叙述正确的是( )
对于可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时C的百分含量与温度(T)和压强(P)关系如图所示,下面叙述正确的是( )| A. | 使用催化剂,C的百分含量增大 | |
| B. | 升温,化学平衡向正反应方向移动 | |
| C. | 化学方程式的化学计量数关系m+n>e+f | |
| D. | 该反应是一个放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| B. | Na2CO3溶液中:2c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| C. | NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO${\;}_{3}^{2-}$) | |
| D. | 常温下,pH=4.75、浓度均为0.1mol•L-1的CH3COOH和CH3OONa混合液:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
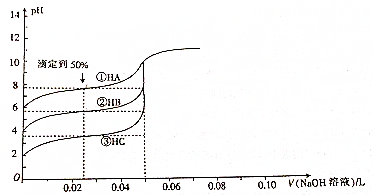
| A. | Ka(HA)>Ka(HB)>Ka(HC) | |
| B. | 滴定到50%时,溶液中:c(A-)>(B-)>(C-) | |
| C. | V(NaOH)溶液=50mL时,溶液中水的电离程度:①>②>③ | |
| D. | V(NaOH)溶液=50mL时,溶液pH的大小关系:pH(A)<pH(B)<pH(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子的半径大小关系:B>C>E | |
| B. | D、E两种元素形成的化合物,可能含有离子键和共价键 | |
| C. | B、D分别和C形成的化合物,都有可能使溴水或品红溶液褪色 | |
| D. | A、B、C三种元素形成的化合物,晶体类型一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
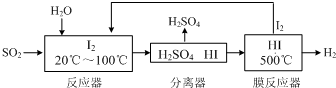
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com