
氧化还原反应在工农业生产和日常生活中有广泛运用。
(1)罐头厂在装食物罐头时通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类防腐剂应具有 ▲ 。 (填“氧化性”或“还原性”);
(2)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,Fe2+更
容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 ▲ 。(填“氧化作用”或“还原作用”);
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。用硫酸
亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 ▲ 。
(4)在下列的空白处填写最适宜的除杂试剂,并写出相应的离子方程式
① FeCl2中含少量FeCl3杂质 ▲ , ▲ 。
② FeCl3中含少量FeCl2杂质 ▲ , ▲ 。
③ FeSO4中含少量CuSO4杂质 ▲ , ▲ 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组物质稀溶液相互反应。无论前者滴入后者,还是后者滴入前者,反应现象都相同的是 ( )
A.Ca(HCO3)2溶液与Ca(OH)2溶液 B.AlCl3溶液与NaOH溶液[
C.KAlO2溶液与KHSO4溶液 D.2%的硝酸银溶液和2%的氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
 N2(g)+3H2(g)
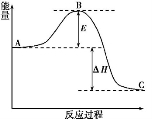
N2(g)+3H2(g) 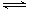 2NH3(g)反应过程的能量变化如下图所示。已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
2NH3(g)反应过程的能量变化如下图所示。已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示 、 ;若该反应使用催化剂,会使图中B点升高还是降低? 。
(2)图中ΔH= kJ·mol-1。
(3)已知恒容时,该体系中各物质浓度随时间变化的曲线如图所示。
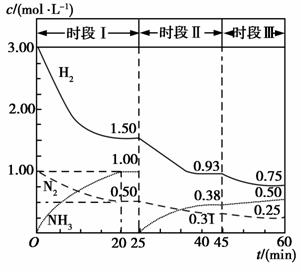
①在0.5 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②45 min时采取的措施是_______________________。
③比较I、II、III时段的化学平衡常数(分别用K1、K2、K3表示)大小________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列几种物质的保存方法中,不正确的是
A.氯化铁溶液保存时加入少量的盐酸
B.氯水保存在棕色瓶里并放在冷暗处
C.漂白粉可以在敞口容器中长期存放
D.溴水盛放在有玻璃塞的细口瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),生成物并不改变的是
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.NaAlO2和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧乙酸是在抗SARS病毒期间常使用的一种高效杀毒剂,其分子式为C2H4O3,它具有氧化性,漂白作用,下列物质中漂白作用原理与过氧乙酸不同的是( )
A.氯水(次氯酸) B.臭氧 C.活性炭 D.过氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.用稀氢氧化钠吸收氯气:2OH-+Cl2=Cl-+ClO-+H2O
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
C.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-=CO2↑+H2O
D.用氢氧化钠溶液除去铝表面的氧化膜:Al(OH)3+OH-=[Al(OH)4] -
查看答案和解析>>
科目:高中化学 来源: 题型:
测得某金属冶炼厂的酸性工业废水中,含有一定量的Fe3+、Cu2+、Au3+等离子。按照“变废为宝”的原则,设计了下图中的回收流程,要求利用常见的酸、碱和工业生产中的废铁屑,从该工业废水中回收金、并生产化工原料铁红和氧化铜。

请你完成下面的问题:
(1)流程图中标号处需加入的相应物质分别是:① ;② ;
③ ;⑤ 。
(2)写出流程图中①处有气体生成的离子方程式: 。
(3)写出流程图中③处发生反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于常温下电解质溶液的叙述中,正确的是( )
A.碳酸氢铵溶液和足量氢氧化钠溶液混合的离子反应:HCO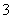 +OH-===CO
+OH-===CO +H2O
+H2O
B.等物质的量浓度、等体积的氨水和盐酸混合后,c(H+)+c(NH )=c(Cl-)+c(OH-)
)=c(Cl-)+c(OH-)
C.等物质的量浓度的NH4Cl溶液和NH3·H2O溶液,溶液中c(NH )前者大于后者
)前者大于后者
D.25℃时,pH=8的0.1 mol·L-1NaX溶液中由水电离出的c(OH-)=1×10-8 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com