
ΓΨΧβΡΩΓΩ»γœ¬ΆΦΘ§άϊ”Ο≈ύ―χΟσΧΫΨΩΑ±ΤχΒΡ–‘÷ ΓΘ Β―ι ±œρNaOHΙΧΧε…œΒΈΦΗΒΈ≈®Α±Υ°Θ§ΝΔΦ¥”ΟΝμ“Μ±μΟφΟσΩέ‘Ύ…œΟφΓΘœ¬±μ÷–Ε‘ Β―ιœ÷œσΥυΉωΒΡΫβ Ά’ΐ»ΖΒΡ «(ΓΓΓΓ)

―Γœν | Β―ιœ÷œσ | ΫβΓΓ Ά |
A | ≈®―ΈΥαΗΫΫϋ≤ζ…ζΑΉ―Χ | NH3”κ≈®―ΈΥαΖ¥”Π≤ζ…ζΝΥΈΔ–ΓΒΡNH4ClΨßΧε |
B | ≈®ΝρΥαΗΫΫϋΈόΟςœ‘œ÷œσ | NH3”κ≈®ΝρΥα≤ΜΖΔ…ζΖ¥”ΠΓΓΓΓ |
C | ¬»Μ·Έο»ή“Κ±δΜκΉ« | ΗΟ»ή“Κ“ΜΕ® «AlCl3»ή“Κ |
D | Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕ | NH3 «“Μ÷÷Ω…»ή–‘Φν |
A. A B. B C. C D. D
ΓΨ¥πΑΗΓΩA
ΓΨΫβΈωΓΩAΓΔNaOHΙΧΧε»ή”ΎΥ°Ζ≈»»Θ§Α±Υ°“ΉΜ”ΖΔΘ§ Β―ι ±œρNaOHΙΧΧε…œΒΈΦΗΒΈ≈®Α±Υ°Θ§Μα≤ζ…ζΑ±ΤχΘ§”κ≈®―ΈΥαΖ¥”Π…ζ≥…¬»Μ·οßΘ§Ζ¥”Πœ÷œσ «”–ΑΉ―Χ…ζ≥…Θ§Ι A’ΐ»ΖΘΜBΓΔΑ±ΤχΈΣΦν–‘ΤχΧεΘ§”κ≈®ΝρΥαΖΔ…ζ÷–ΚΆΖ¥”Π…ζ≥…ΝρΥαοßΘ§Ι B¥μΈσΘΜCΓΔΑ±Τχ”ꬻ̷ΈοΖΔ…ζΗ¥Ζ÷ΫβΖ¥”Π…ζ≥…«β―θΜ·ΈοΘ§»γ¬»Μ·Έο»ή“Κ±δΜκΉ«Θ§Ω…Ρή…ζ≥…Ρ―»ή–‘«β―θΜ·ΈοΘ§ΒΪ≤Μ“ΜΕ®ΈΣAl(OH)3Θ§“≤Ω…ΡήΈΣMg(OH)2Β»≥ΝΒμΘ§Ι C¥μΈσΘΜDΓΔΑ±Τχ Ι Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕΒΡ‘≠“ρ «”κΥ°Ζ¥”Π…ζ≥…NH3H2OΘ§Βγάκ…ζ≥…OH-άκΉ”Θ§»ή“Κ≥ Φν–‘Θ§ΒΪΑ±ΤχΈΣΖ«ΒγΫβ÷ Θ§≤Μ τ”ΎΦνΘ§Ι D¥μΈσΘΜΙ ―ΓAΓΘ


 –Γ―ßΕαΙΎABΨμœΒΝ–¥πΑΗ
–Γ―ßΕαΙΎABΨμœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ500Γφ ±Θ§ΫΪΉψΝΩΒΡAΙΧΧεΆΕ»κ2.0L’φΩ’Οή±’»ίΤς÷–Θ§
ΖΔ…ζAΘ®sΘ©![]() 2BΘ®gΘ©+CΘ®gΘ©Ζ¥”ΠΘ§≤βΒΟΤχΧεCΥφ ±ΦδΒΡ≈®Ε»±δΜ·»γœ¬ΆΦΥυ Ψ
2BΘ®gΘ©+CΘ®gΘ©Ζ¥”ΠΘ§≤βΒΟΤχΧεCΥφ ±ΦδΒΡ≈®Ε»±δΜ·»γœ¬ΆΦΥυ Ψ

Θ®1Θ©“―÷ΣΗΟΖ¥”Π÷Μ”–ΗΏΈ¬œ¬ΡήΉ‘ΖΔΫχ––Θ§‘ρΗΟΖ¥”ΠΒΡΓςH 0Θ®ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑΘΫΓ±Θ©ΓΘ
Θ®2Θ©‘Ύ…œ ωΖ¥”ΠΧθΦΰœ¬Θ§¥”Ζ¥”ΠΩΣ ΦΒΫΤΫΚβΘ§”ΟB±μ ΨΒΡΜ·―ßΖ¥”ΠΥΌ¬ ΈΣvΘ®BΘ©= molΓΛL-1ΓΛmin-1Θ§500Γφ ±ΒΡΤΫΚβ≥Θ ΐK= ΘΜ
Θ®3Θ©ΦΉΆι «“Μ÷÷≥ΘΦϊΒΡ«εΫύΡή‘¥ΘΚ
ΔΌ»τ800 Γφ ±Θ§Ζ¥”ΠCH4Θ®gΘ©ΘΪH2OΘ®gΘ©![]() COΘ®gΘ©ΘΪ3H2Θ®gΘ© ΠΛHΘΫΘΪ206.1 kJΓΛmolΘ≠1ΒΡΤΫΚβ≥Θ ΐΘ®KΘ©ΘΫ1.0Θ§Ρ≥ ±ΩΧ≤βΒΟΗΟΈ¬Ε»œ¬Οή±’»ίΤς÷–ΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ≈®Ε»»γœ¬±μΘΚ
COΘ®gΘ©ΘΪ3H2Θ®gΘ© ΠΛHΘΫΘΪ206.1 kJΓΛmolΘ≠1ΒΡΤΫΚβ≥Θ ΐΘ®KΘ©ΘΫ1.0Θ§Ρ≥ ±ΩΧ≤βΒΟΗΟΈ¬Ε»œ¬Οή±’»ίΤς÷–ΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ≈®Ε»»γœ¬±μΘΚ
CH4 | H2O | CO | H2 |
3.0 molΓΛLΘ≠1 | 8.5 molΓΛLΘ≠1 | 2.0 molΓΛLΘ≠1 | 2.0 molΓΛLΘ≠1 |
‘ρ¥Υ ±’ΐΓΔΡφΖ¥”ΠΥΌ¬ ΒΡΙΊœΒ « ΓΘΘ®Χν±ξΚ≈Θ©
AΘ°vΘ®’ΐΘ©<vΘ®ΡφΘ© BΘ°vΘ®’ΐΘ©ΘΫvΘ®ΡφΘ© CΘ°vΘ®’ΐΘ©>vΘ®ΡφΘ© DΘ°ΈόΖ®≈–Εœ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ ΒΡΥ°»ή“Κ“ρΥ°Ϋβ≥ Υα–‘ΒΡ «
A. NaHSO4 B. NaHCO3 C. NH4Cl D. SO2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΣ―–ΨΩΫπ τΗ· ¥ΒΡΧθΦΰΚΆΥΌ¬ Θ§Ρ≥ΩΈΆβ–ΓΉι―ß…ζ”ΟΫπ τΥΩΫΪ»ΐΗυ¥σ–ΓœύΆ§ΒΡΧζΕΛΖ÷±πΙΧΕ®‘ΎΆΦ ΨΒΡ»ΐΗωΉΑ÷Ο÷–Θ§‘ΌΖ≈÷Ο”Ύ≤ΘΝß÷”’÷άο±Θ¥φœύΆ§ΒΡ“ΜΕΈ ±ΦδΓΘœ¬Ν–Ε‘ Β―ιΫα χ ±œ÷œσΒΡΟη ω≤Μ’ΐ»ΖΒΡ «( )
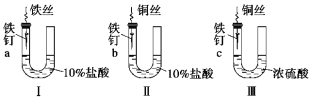
AΘ°ΉΑ÷ΟΔώΉσ≤ύΒΡ“ΚΟφ“ΜΕ®Μαœ¬ΫΒ BΘ°Ήσ≤ύ“ΚΟφΉΑ÷ΟΔώ±»ΉΑ÷ΟΔρΒΡΒΆ
CΘ°ΉΑ÷ΟΔρ÷–ΒΡΧζΕΛΗ· ¥Ήν―œ÷Ί DΘ°ΉΑ÷ΟΔσ÷–ΒΡΧζΕΛΦΗΚθΟΜ±ΜΗ· ¥
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΥφΉ≈»ΥΟ«…ζΜνΫΎΉύΒΡΦ”ΩλΘ§ΖΫ±ψΒΡ–ΓΑϋΉΑ ≥ΤΖ“―±ΜΙψΖΚΫ” ήΘ§ΈΣΝΥΖά÷ΙΗ± ≥ΤΖ―θΜ·±δ÷ Θ§―”≥Λ ≥ΤΖΒΡ±Θ÷ ΤΎΘ§‘ΎΑϋΉΑ¥ϋ÷–≥ΘΖ≈»κΩΙ―θΜ·Έο÷ Θ°œ¬Ν–≤Μ τ”ΎΩΙ―θΜ·Έο÷ ΒΡ «Θ® Θ©
A.…ζ ·Μ“
B.―«ΝρΥαΡΤΘ®Na2SO3Θ©
C.ΧζΖέ
D.ΝρΥα―«ΧζΘ®FeSO4Θ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύœ¬Ν–≤ΌΉς÷–Θ§“ΜΑψ«ιΩωœ¬≤ΜΡήœύΜΞΫ”¥ΞΒΡ «Θ® Θ©
A. ”ΟΫΚΆΖΒΈΙήœρ ‘ΙήΡΎΒΈΦ”“ΚΧε ±Θ§ΫΚΆΖΒΈΙήΦβΕΥ”κ ‘ΙήΡΎ±Ύ
B. Ζ÷“Κ ±Θ§Ζ÷“Κ¬©ΕΖœ¬ΕΥ”κ…’±≠ΡΎ±Ύ
C. Ιΐ¬Υ ±Θ§…’±≠ΡΎ±Ύ”ꬩΕΖœ¬ΕΥ
D. Ιΐ¬Υ ±Θ§≤ΘΝßΑτ”κ»ΐ≤ψ¬Υ÷Ϋ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25Γφ ±Θ§œρ10 mL 0.1 molΓΛL-1 NH4HSO4»ή“Κ÷–÷πΒΈΒΈ»κ0.1 molΓΛL-1 NaOH»ή“ΚΘ§»ή“ΚΒΡpH”κNaOH»ή“ΚΧεΜΐΙΊœΒ»γ”“ΆΦΥυ ΨΘΚ
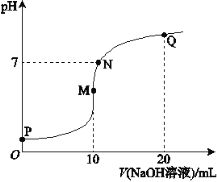
(1)”ΟΒγάκΖΫ≥Χ Ϋ±μ ΨPΒψpHΘΦ7ΒΡ‘≠“ρ «________ΓΘ
(2)MΓΔQΝΫΒψ÷–Θ§Υ°ΒΡΒγάκ≥ΧΕ»Ϋœ¥σΒΡ «________ΒψΓΘ
(3)œ¬Ν–ΙΊœΒ÷–Θ§’ΐ»ΖΒΡ «________ΓΘ
a.MΒψc(Na+)ΘΨc(NH4+)
b.NΒψc(NH4+)+c(Na+)=2c(SO42-)
c.QΒψc(NH4+)+c(NH3ΓΛH2O)=c(Na+)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΣΝΥ―–ΨΩΜ·―ßΖ¥”ΠA+B=C+DΒΡΡήΝΩ±δΜ·«ιΩωΘ§Ρ≥Ά§―ß…ηΦΤΝΥ»γΆΦΥυ ΨΉΑ÷ΟΓΘΒ±œρ Δ”–AΒΡ ‘Ιή÷–ΒΈΦ” ‘ΦΝB ±Θ§Ω¥ΒΫU–ΈΙή÷–ΦΉ¥Π“ΚΟφœ¬ΫΒ““¥Π“ΚΟφ…œ…ΐΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ

Θ®1Θ©ΗΟΖ¥”ΠΈΣ_______Ζ¥”ΠΘ®ΧνΓΑΖ≈»»Γ±ΜρΓΑΈϋ»»Γ±Θ©ΓΘ
Θ®2Θ©AΚΆBΒΡΉήΡήΝΩ±»CΚΆDΒΡΉήΡήΝΩ_______Θ®ΧνΓΑΗΏΓ±ΜρΓΑΒΆΓ·Γ·Θ©ΓΘ
Θ®3Θ©Ζ¥”ΠΈοΜ·―ßΦϋΕœΝ―Έϋ ’ΒΡΡήΝΩ____Θ®ΧνΓΑΗΏΓ·Γ·ΜρΓΑΒΆΓ·Γ·Θ©”Ύ…ζ≥…ΈοΜ·―ßΦϋ–Έ≥…Ζ≈≥ωΒΡΡήΝΩΓΘ
Θ®4Θ©–¥≥ω“ΜΗωΖϊΚœΧβ÷–ΧθΦΰΒΡΜ·―ßΖΫ≥Χ ΫΘΚ______________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com