
已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCNFe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是( )
A.向溶液中加入少许KCl固体,溶液颜色变浅
B.升高温度,平衡一定发生移动
C.加入少许KCl固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反
D.平衡常数表达式为K=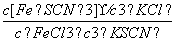
科目:高中化学 来源: 题型:
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:
①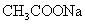 与
与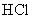 ;②
;②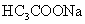 与NaOH
与NaOH
③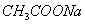 与
与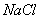 ④
④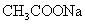 与
与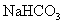 下列各项排序正确的是( )
下列各项排序正确的是( )
A.pH:②>③>④>① B 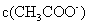 :②>④>③>①
:②>④>③>①
C.溶液中:①>③>②>④ D 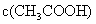 :①>④>③>②
:①>④>③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物Ⅰ可以用E和H在一定条件下合成:
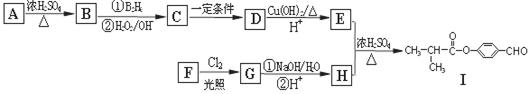
请根据以下信息完成下列问题:
①A为丁醇且核磁共振氢谱有2种不同化学环境的氢;
②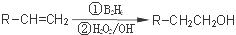
③一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)B的分子式为: 。
(2)C→D的反应类型为
(3)芳香族化合物F的分子式为C7H8O, 苯环上的一氯代物只有两种,则F的结构简式为: 。
(4)D生成E的化学方程式为 。
E与H反应生成I的方程式为 。
(5)I的同系物K相对分子质量比I小28。K的结构中能同时满足如下条件:①苯环上只有两个取代基;②分子中不含甲基。共有 种(不考虑立体异构)。试写出上述同分异构体中任意一种消耗NaOH最多的有机物结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)===2AB3(g) 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)。下列判断正确的是( )
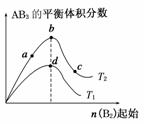
A.在T2和n(A2)不变时达到平衡,AB3的物质的量大小 为:c>b>a
B.若T2>T1,则正反应一定是放热反应
C.达到平衡时A2的转化率大小为:b>a>c
D.若T2>T1,达到平衡时b、d点的反应速率为vd>vb
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使得甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.8 | 1.24 | ? |
①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的转化率和浓度的曲线示意图。

(2)在直接以甲醚为燃料的电池中,电解质溶液为酸性,负极的反应为________________、正极的反应为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2AH++HA-,HA-H++A2-。
(1)相同浓度下,NaHA溶液的pH________(填“大于”、“小于”或“等于”) Na2A溶液的pH。
(2)某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是________。
a.c(H+)·c(OH-)=1×10-14
b.c(Na+)+c(K+)=c(HA-)+2c(A2-)
c.c(Na+)>c(K+)
d.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s)Ca2+(aq)+A2-(aq) ΔH>0。
①降低温度时,Ksp________(填“增大”“减小”或“不变”)。
②滴加少量浓盐酸,c(Ca2+)________(填“增大”“减小”或“不变”)。
Ⅱ.含有Cr2O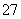 的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O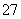 。为使废水能达标排放,作如下处理:Cr2O
。为使废水能达标排放,作如下处理:Cr2O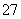
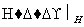 Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
Cr3+、Fe3+石灰水,Cr(OH)3、Fe(OH)3
(1)该废水中加入绿矾(FeSO4·7H2O)和稀硫酸,发生反应的离子方程式为
________________________________________________________________________。
(2)欲使10 L该废水中的Cr2O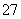 完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
完全转化为Cr3+,理论上需要加入________g FeSO4·7H2O。
(3)若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为________。(已知:
Ksp=4.0×10-38 Ksp=6.0×10-31)
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两种化合物都只含X、Y两种元素,甲、乙中X元素的百分含量分别为30.4%和25.9%.若已知甲的分子式是XY2,则乙的分子式只可能是()
| A. | XY | B. | X2Y | C. | X2Y3 | D. | X2Y5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
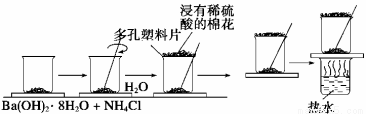
在一个小烧杯里,加入约20 g已研磨成粉末的氢氧化钡晶体,将小烧杯放在事先已滴有3—4滴水的玻璃片上,然后再加入约10 g NH4Cl晶体,并立即用玻璃棒迅速搅拌。试完成下列问题:
(1)写出有关反应方程式 ,该反应属于 反应。(填基本反应类型)
(2)实验中要立即用玻璃棒迅速搅拌的原因是__ 。
(3)如果实验中没有看到“结冰”现象,可能的原因是(列举三条) 。
(4)“结冰”现象说明了该反应是 热(填“放”或“吸”),反应物的总能量比生成物的总能量 (填“高”或“低”);
(5)在上述实验过程中,用浸有稀硫酸的湿棉花置于多孔塑料板上的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com